摘要:(一)化学反应速率 1. 概念: 化学反应进行的快慢定量描述--化学反应速率----在反应中.某物质的浓度随时间的变化率 2表示:一般用单位时间内某一种反应物或生成物的物质的量浓度的变化值来表示. 表达式: vi=ΔC/Δt 单位: mol/等. 3. 注意 (1) 以上所指的反应速率是平均反应速率而不是瞬时反应速率. (2) 同一反应在不同时刻.瞬时反应速率不同. (3) 同一反应在不同时间内.平均反应速率不同. (4) 同一反应在同一时间内.用不同物质来表示的反应速率可能不同. (5) 中学阶段计算的是平均反应速率.图示的应是瞬时速率. 3. 规律 对于同一反应:mA+qD(g) 同一时间:vA:vB:vC:vD =ΔnA:ΔnB:ΔnC:ΔnD =ΔCA:ΔCB:ΔCC:ΔCD =m:n:p:q 浓 度 c1 c2 即反应速率的数值之比等于这些物质在化学方程式中的化学计量数之比. 4. 图示 对于一般反应: aA + bB ==== cC + dD 反应物A的浓度随时间的变化曲线如图所示. 在t1~t2内.平均反应速率以A的浓度变化 表示为: v /Δt = -(c2-c1)/(t2-t1) 对于某一反应.各反应物或生成物的起始浓度是不一定的.但在同一时间内各物质的浓度变化(ΔC)却是一定的.作浓度图一定要符合这一变化规律 如: 有关2SO2+O2 2SO3反应的下列图象正确的是( ) 抓住规律:V(so2)∶V(o2)∶V(so3)=2∶1∶2 ΔC(so2)∶ΔC(o2)∶ΔC(so3)=2∶1∶2 另外.对一可逆可应.必须同一时刻达到化学平衡.所以正确答案:B
网址:http://m.1010jiajiao.com/timu3_id_351065[举报]
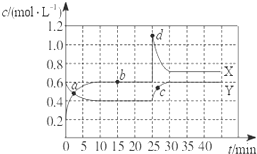 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化,则下列说法不正确的是( )
查看习题详情和答案>>
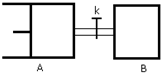 如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)?2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )
如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB=aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X(g)+Y(g)?2Z(g)+W(g)达到平衡时,VA=1.2aL,则下列说法正确的是( )| A、反应开始时,B容器中化学反应速率快 | B、A容器中X的转化率为40%,且比B容器中X的转化率小 | C、打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计) | D、打开K达新平衡后,升高B容器温度,A容器体积一定增大 |
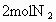 和
和 发生反应:
发生反应: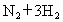

 ,2min时,测得剩余
,2min时,测得剩余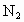 为1mol,对于这一化学反应速率表示不正确的是
为1mol,对于这一化学反应速率表示不正确的是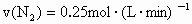



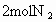 和
和 发生反应:
发生反应:

 ,2min时,测得剩余
,2min时,测得剩余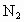 为1mol,对于这一化学反应速率表示不正确的是
为1mol,对于这一化学反应速率表示不正确的是


