网址:http://m.1010jiajiao.com/timu3_id_350105[举报]
(16分)观察下列部分图形,并按要求回答下列问题
(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取
杂化轨道形成σ键,每个晶胞中含碳原子数为 个。
(2)白磷分子(P4)中键角为 ,分子的空间结构为 ,每1mol白磷分子含 mol P-P共价键。若将1分子白磷中所有P-P键打开并各插入一个氧原子所得氧化物的分子式为 ,若每个P原子的孤对电子再与氧原子配位,就可得到磷的另一种氧化物 (填分子式)。
(3)由SiO2晶体结构知SiO2晶体是 晶体,每1mol SiO2晶体含 mol Si-O共价键。
(4)已知CaC2晶体的晶胞结构与NaCl晶体相似,(如图)但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长,则CaC2晶体中Ca2+配位数(C.N)为 。C22-与O22+互为等电子体,O22+的电子式为 ,1molO22+中含π键数目为 。
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,观察图形回答。这个基本结构单元由 个硼原子组成,共含有 个B-B键。
(6)若测得mg NaCl固体的体积为Vcm3,已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm,则阿佛加德罗常数![]() 的表达式为 。
的表达式为 。
查看习题详情和答案>>
(16分)观察下列部分图形,并按要求回答下列问题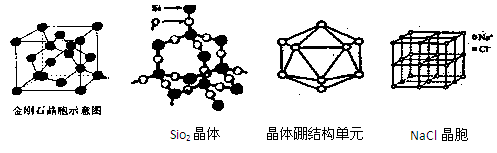
(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取
杂化轨道形成σ键,每个晶胞中含碳原子数为 个。
(2)白磷分子(P4)中键角为 ,分子的空间结构为 ,每1mol白磷分子含 mol P-P共价键。若将1分子白磷中所有P-P键打开并各插入一个氧原子所得氧化物的分子式为 ,若每个P原子的孤对电子再与氧原子配位,就可得到磷的另一种氧化物 (填分子式)。
(3)由SiO2晶体结构知SiO2晶体是 晶体,每1mol SiO2晶体含 mol Si-O共价键。
(4)已知CaC2晶体的晶胞结构与NaCl晶体相似,(如图)但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长,则CaC2晶体中Ca2+配位数(C.N)为 。C22-与O22+互为等电子体,O22+的电子式为 ,1molO22+中含π键数目为 。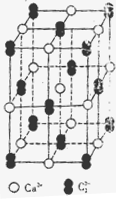
(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,观察图形回答。这个基本结构单元由 个硼原子组成,共含有 个B-B键。
(6)若测得mg NaCl固体的体积为Vcm3,已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm,则阿佛加德罗常数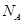 的表达式为 。
的表达式为 。
(16分)观察下列部分图形,并按要求回答下列问题
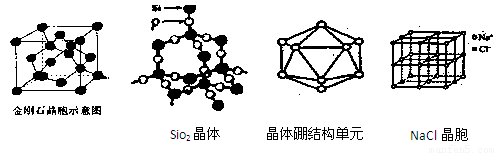
(1)由金刚石晶体结构和晶胞图知,金刚石是原子晶体,晶体中碳原子取
杂化轨道形成σ键,每个晶胞中含碳原子数为 个。
(2)白磷分子(P4)中键角为 ,分子的空间结构为 ,每1mol白磷分子含 mol P-P共价键。若将1分子白磷中所有P-P键打开并各插入一个氧原子所得氧化物的分子式为 ,若每个P原子的孤对电子再与氧原子配位,就可得到磷的另一种氧化物 (填分子式)。
(3)由SiO2晶体结构知SiO2晶体是 晶体,每1mol SiO2晶体含 mol Si-O共价键。
(4)已知CaC2晶体的晶胞结构与NaCl晶体相似,(如图)但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长,则CaC2晶体中Ca2+配位数(C.N)为 。C22-与O22+互为等电子体,O22+的电子式为 ,1molO22+中含π键数目为 。

(5)晶体硼的基本结构单元都是由硼原子组成的正二十面体的原子晶体。其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,观察图形回答。这个基本结构单元由 个硼原子组成,共含有 个B-B键。
(6)若测得mg NaCl固体的体积为Vcm3,已知NaCl晶体中,靠得最近的Na+、Cl-间的距离为a cm,则阿佛加德罗常数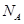 的表达式为 。
的表达式为 。
查看习题详情和答案>>
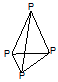
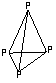 则P4分子中共有___________个P―P键。
则P4分子中共有___________个P―P键。