摘要:21.吸收HCl用:a d e h i k l 吸收NH3不宜采用:h i.因为h中盛有碱石灰与NH3不反应,NH3比空气轻.在导管口处向空气中扩散.所以不用i.
网址:http://m.1010jiajiao.com/timu3_id_349846[举报]
(2010?上海)CaCO3广泛存在于自然界,是一种重要的化工原料.大理石主要成分为CaCO3,另外有少量的含硫化合物.实验室用大理石和稀盐酸反应制备CO2气体.下列装置可用于CO2气体的提纯和干燥.

完成下列填空:
1)用浓盐酸配制1:1(体积比)的稀盐酸(约6mol.L-1),应选用的仪器是
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
2)上述装置中,A是
3)上述装置中,B中物质是
4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重为了将石蜡和碳酸钙溶出,应选用的试剂是
a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正已烷
5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出
6)上述测定实验中,连续
查看习题详情和答案>>

完成下列填空:
1)用浓盐酸配制1:1(体积比)的稀盐酸(约6mol.L-1),应选用的仪器是
abc
abc
.a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
2)上述装置中,A是
CuSO4溶液或酸性KMnO4溶液
CuSO4溶液或酸性KMnO4溶液
溶液,NaHCO3溶液可以吸收HCl气体或吸收酸性气体
HCl气体或吸收酸性气体
.3)上述装置中,B中物质是
无水CaCl2
无水CaCl2
.用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果偏低
偏低
(填“偏高”、“偏低”或“不受影响”).4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重为了将石蜡和碳酸钙溶出,应选用的试剂是
bd
bd
.a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正已烷
5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出
石蜡
石蜡
后溶出CaCO3
CaCO3
.6)上述测定实验中,连续
两次称量的结果相差不超过(或小于)0.001g
两次称量的结果相差不超过(或小于)0.001g
,说明样品已经恒重.(2012?太原一模)氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品.某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体
(CuCl2?2H2O).

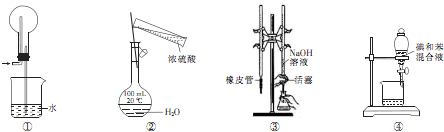
(1)实验室采用如图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去).
①仪器A的名称是
②装置B中发生反应的离子方程式是
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)
(2)试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b.NH3?H2O c.CuO d.Cu2(OH)2CO3 e.CuSO4
(3)在溶液2转化为CuCl2?2H2O的操作过程中,发现溶液颜色由蓝色变为绿色.小组同学欲探究其原因.
已知:在氯化铜溶液中有如下转化关系:Cu(H2O)42+(aq)+4Cl-(aq) CuCl42-(aq)+4H2O(l)
CuCl42-(aq)+4H2O(l)
蓝色 黄色
①上述反应的化学平衡常数表达式是K=
.若增大氯离子浓度,K值(填“增大”、“减小”或“不变”)
②取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号)
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失.
查看习题详情和答案>>
(CuCl2?2H2O).

(1)实验室采用如图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去).

①仪器A的名称是
分液漏斗
分液漏斗
.②装置B中发生反应的离子方程式是
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
③有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)
否
否
.(2)试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)
cd
cd
.a.NaOH b.NH3?H2O c.CuO d.Cu2(OH)2CO3 e.CuSO4
(3)在溶液2转化为CuCl2?2H2O的操作过程中,发现溶液颜色由蓝色变为绿色.小组同学欲探究其原因.
已知:在氯化铜溶液中有如下转化关系:Cu(H2O)42+(aq)+4Cl-(aq)
 CuCl42-(aq)+4H2O(l)
CuCl42-(aq)+4H2O(l)蓝色 黄色
①上述反应的化学平衡常数表达式是K=
c(Cu
| ||
c[Cu
|
c(Cu
| ||
c[Cu
|
不变
不变
.②取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能够证明CuCl2溶液中有上述转化关系的是(填序号)
abc
abc
.a.将Y稀释,发现溶液呈蓝色
b.在Y中加入CuCl2晶体,溶液变为绿色
c.在Y中加入NaCl固体,溶液变为绿色
d.取Y进行电解,溶液颜色最终消失.
(1)如图所示是分离混合物时常用的仪器,回答下列问题:

①写出仪器C、E的名称
②分离以下混合物应该主要选用上述什么仪器?(填一个字母符号)
粗盐和泥沙:
③若向C装置中加入碘水和足量CCl4,充分振荡后静置,会观察到什么现象?
(2)请根据所提供的试剂和仪器,按要求填空:

①气体发生装置A可用来制取氧气,若用E装置收集氧气完毕时,应先
②实验室用大理石固体与稀盐酸制备二氧化碳气体,选用上述装置中的
a.NaHCO3溶液 b.NaOH溶液 c.澄清石灰水 d.浓硫酸.
查看习题详情和答案>>

①写出仪器C、E的名称
分液漏斗
分液漏斗
、冷凝管
冷凝管
②分离以下混合物应该主要选用上述什么仪器?(填一个字母符号)
粗盐和泥沙:
B
B
花生油和水:C
C
③若向C装置中加入碘水和足量CCl4,充分振荡后静置,会观察到什么现象?
分液漏斗内液体分两层,上层液体无色,下层液体紫红色
分液漏斗内液体分两层,上层液体无色,下层液体紫红色
(2)请根据所提供的试剂和仪器,按要求填空:

①气体发生装置A可用来制取氧气,若用E装置收集氧气完毕时,应先
b
b
后a
a
(a.熄灭酒精灯,b.从水中取出导气管,填序号,下同).②实验室用大理石固体与稀盐酸制备二氧化碳气体,选用上述装置中的
B
B
(填序号)作为发生装置;盐酸具有挥发性,二氧化碳气体中含有少量的氯化氢气体,可以用上图中的F装置除去HCl气体(F洗气瓶可吸收HCl气体,不吸收CO2气体,顺利使CO2气体进入下一个装置).实验中含有杂质的气体应该从a
a
(填“a”或“b”)口进入洗气瓶,洗气瓶中应装a
a
(填序号a、b、c或d)a.NaHCO3溶液 b.NaOH溶液 c.澄清石灰水 d.浓硫酸.
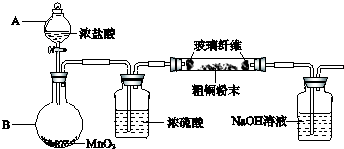
(2012?重庆)氯离子插层镁铝水滑石[Mg2Al(OH)6Cl?xH2O]是一种新型离子交换材料,其在高温下完全分解为MgO、Al2O3、HCl和水蒸气.现用如图装置进行实验确定其化学式(固定装置略去).
(1)Mg2Al(OH)6Cl?xH2O热分解的化学方程式为
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为
(3)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是
(4)完全分解后测得C增重3.65g、D增重9.90g,则x=
(5)上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1-2x(CO3)y?zH2O],该生成物能发生类似的热分解反应.现以此物质为样品,用(2)中连接的装置和试剂进行实验测定z,除测定D的增重外,至少还需测定
查看习题详情和答案>>

(1)Mg2Al(OH)6Cl?xH2O热分解的化学方程式为
2[Mg2Al(OH)6Cl?xH2O]
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑
| ||
2[Mg2Al(OH)6Cl?xH2O]
4MgO+Al2O3+2HCl↑+(5+2x)H2O↑
.
| ||
(2)若只通过测定装置C、D的增重来确定x,则装置的连接顺序为
a→e→d→b
a→e→d→b
(按气流方向,用接口字母表示),其中C的作用是吸收HCl气体
吸收HCl气体
.装置连接后,首先要进行的操作的名称是检查装置的气密性
检查装置的气密性
.(3)加热前先通N2排尽装置中的空气,称取C、D的初始质量后,再持续通入N2的作用是
将分解产生的气体全部带入装置C、D中完全吸收
将分解产生的气体全部带入装置C、D中完全吸收
、防止产生倒吸
防止产生倒吸
等.(4)完全分解后测得C增重3.65g、D增重9.90g,则x=
x
x
.若取消冷却玻管B后进行实验,测定的x值将偏低
偏低
(填“偏高”或“偏低”).(5)上述水滑石在空气中放置时易发生反应生成[Mg2Al(OH)6Cl1-2x(CO3)y?zH2O],该生成物能发生类似的热分解反应.现以此物质为样品,用(2)中连接的装置和试剂进行实验测定z,除测定D的增重外,至少还需测定
装置C的增重及样品质量(或样品质量及样品分解后残余物质量或装置C的增重及样品分解后残余物质量)
装置C的增重及样品质量(或样品质量及样品分解后残余物质量或装置C的增重及样品分解后残余物质量)
.