网址:http://m.1010jiajiao.com/timu3_id_349796[举报]
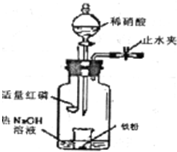 某同学用如图装置进行铁和稀硝酸反应的实验探究,实验步骤为:
某同学用如图装置进行铁和稀硝酸反应的实验探究,实验步骤为:A.向广口瓶内注入足量热NaOH溶液,将盛有ag纯铁粉的小烧杯放入瓶中.
B.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞.
C.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入120ml 6mol/L的稀硝酸,铁粉恰好完全溶解.
(一)气体产物成分探究
①燃烧红磷的目的
②为证明气体产物为NO,该同学在步骤c后打开止水夹,
向瓶内通入少量氧气,该反应的化学方程式为
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物中只有+2价铁;
假设2:
假设3:
(2)请根据以下操作填写预期现象和结论:
| 实验操作 | 预期现象 | 结论 |
| 分别取小烧杯中反应后溶液装入甲、乙两支试管,在甲中滴加紫色的酸性KMnO4溶液;在乙中滴加KSCN溶液 | ||
Ⅰ.下列有关操作正确的是 _。
①FeBr3作催化剂,苯和溴水发生反应可生成无色、比水重的液体溴苯
②将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,实现乙醇被氧化为乙醛的实验
③用Cu和Ag作为两极,H2SO4溶液作为电解质溶液,可以构成原电池
④为了防止自来水管生锈,一般在表面镀上一层Zn
⑤使用AgNO3溶液验证三氯甲烷中是否含有氯元素,现象是产生白色沉淀
A.②④ B.①② C.③⑤ D.④⑥
Ⅱ. 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用右图的装置制备乙酸乙酯。

(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用
是: 。
(2)已知下表数据:
|
物质 |
熔点/℃ |
沸点/℃ |
密度/(g/cm3) |
|
乙醇 |
-144 |
78 |
0.789 |
|
乙酸 |
16.6 |
117.9 |
1.05 |
|
乙酸乙酯 |
-83.6 |
77.5 |
0.90 |
|
浓硫酸 |
—— |
338 |
1.84 |
①按装置图安装好仪器后,需要试剂为3 ml 乙醇,2 ml乙酸,适量浓硫酸,请选择合适的加入顺序 。
A. 先加浓硫酸,再加乙醇,最后加乙酸
B. 先加乙醇,再加浓硫酸,最后加乙酸
C. 先加乙酸,再加浓硫酸,最后加乙醇
D. 先加浓硫酸,再加乙酸,最后加乙醇
②根据上表数据分析,为什么乙醇需要过量一些,其原因是 。
(3)按正确操作重新实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物。现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。在图中圆括号表示加入适当的试剂,编号表示适当的分离方法。
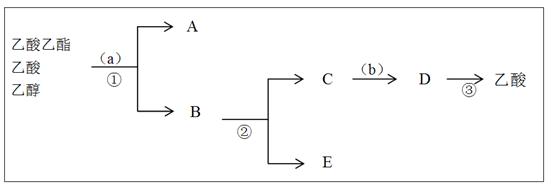
①写出加入的试剂名称: 试剂(a)是 ;试剂(b)是 。
②写出有关的操作分离方法:①是 ,②是 ,③是 。
查看习题详情和答案>>
Ⅰ.下列有关操作正确的是 _。
①FeBr3作催化剂,苯和溴水发生反应可生成无色、比水重的液体溴苯
②将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,实现乙醇被氧化为乙醛的实验
③用Cu和Ag作为两极,H2SO4溶液作为电解质溶液,可以构成原电池
④为了防止自来水管生锈,一般在表面镀上一层Zn
⑤使用AgNO3溶液验证三氯甲烷中是否含有氯元素,现象是产生白色沉淀
A.②④ B.①② C.③⑤ D.④⑥
Ⅱ. 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用右图的装置制备乙酸乙酯。
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用
是: 。
(2)已知下表数据:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | —— | 338 | 1.84 |
A. 先加浓硫酸,再加乙醇,最后加乙酸
B. 先加乙醇,再加浓硫酸,最后加乙酸
C. 先加乙酸,再加浓硫酸,最后加乙醇
D. 先加浓硫酸,再加乙酸,最后加乙醇
②根据上表数据分析,为什么乙醇需要过量一些,其原因是 。
(3)按正确操作重新实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物。现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。在图中圆括号表示加入适当的试剂,编号表示适当的分离方法。

①写出加入的试剂名称: 试剂(a)是 ;试剂(b)是 。
②写出有关的操作分离方法:①是 ,②是 ,③是 。 查看习题详情和答案>>
Ⅰ.下列有关操作正确的是 _。
①.FeBr3作催化剂,苯和溴水发生反应可生成无色、比水重的液体溴苯
②.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,实现乙醇被氧化为乙醛的实验
③.用Cu和Ag作为两极,H2SO4溶液作为电解质溶液,可以构成原电池
④.为了防止自来水管生锈,一般在表面镀上一层Zn
⑤.使用AgNO3溶液验证三氯甲烷中是否含有氯元素,现象是产生白色沉淀
A.②④ B.①② C.③⑤ D.④⑥
Ⅱ. 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用右图的装置制备乙酸乙酯。

(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用
是: 。
(2)已知下表数据:ks5u
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | —— | 338 | 1.84 |
①按装置图安装好仪器后,需要试剂为3 ml 乙醇,2 ml乙酸,适量浓硫酸,请选择合适的加入顺序 。
A. 先加浓硫酸,再加乙醇,最后加乙酸
B. 先加乙醇,再加浓硫酸,最后加乙酸
C. 先加乙酸,再加浓硫酸,最后加乙醇
D. 先加浓硫酸,再加乙酸,最后加乙醇
②根据上表数据分析,为什么乙醇需要过量一些,其原因是 。
(3)按正确操作重新实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物。现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。在图中圆括号表示加入适当的试剂,编号表示适当的分离方法。

①写出加入的试剂名称: 试剂(a)是 ;试剂(b)是 。
②写出有关的操作分离方法:①是 ,②是 ,③是 。
查看习题详情和答案>> 火柴头中硫元素、氯元素的检验
火柴头中硫元素、氯元素的检验
【实验情景】
实验一:取两只洁净的小烧杯,标记为甲、乙,在乙烧杯中加入10ml 0.01mol?L-1KMnO4酸性溶液。将两根火柴伸入甲烧杯里,再用一根燃着的火柴点燃火柴头(如右图所示),待火柴头燃尽,即将火柴移出,迅速将甲烧杯倒扣在乙烧杯上,轻轻振荡乙烧杯,观察实验现象。
实验二:用漏斗、试管、注射器、导管等组成如右图装置,将两 根火柴放在漏斗下面,用一根燃着的火柴点燃火柴头,使火柴头燃烧。慢慢拉动注射器的活塞进行抽气,让火柴头燃烧产生的气体通过 0.01mol?L-1KMnO4酸性溶液,观察实验现象。
0.01mol?L-1KMnO4酸性溶液,观察实验现象。
实验三:将燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于 试管中,滴加AgNO3和稀硝酸,观察实验现象。
实验四:将3-4根火柴头摘下浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,观察实验现象。
【问题设计】
问题1:安全火柴盒侧面涂有红磷(发火剂)和Sb2O3(易燃物)等,火柴头上的物质一般是 、 等氧化剂和 等易燃物。
问题2:实验一和实验二均可观察到的实验现象是 ,请用化学方程式说明产生这种现象的原因 。
实验一设计的方案还利用了SO2的一种 性质。
问题3:写出以下反应的化学方程式:
(1) 将SO2通入氯水中,浅黄绿色褪成无色
体现了SO2的 性。
(2) 将SO2通入溴水中,红棕色褪为无色
体现了SO2的 性。
(3) 将SO2通入无色的氢硫酸溶液,溶液变浑浊
体现了SO2的 性。
问题4:实验三可观察到白色沉淀 产生,说明将燃尽的火柴头浸泡在少量水中,会有 物质被浸出,产生该物质的反应方程式为 ,
主要是把火柴头中含有的 转化为 。
问题5:实验四产生的白色沉淀为 ,NaNO2的作用是 ,
反应的离子方程式为 。
查看习题详情和答案>>