摘要:镁橄榄石(MgO·2SiO2)中的阴离子是: ( ) A.SiO32- B.Si2O52- C.SiO44- D.Si4O104- Ⅱ卷 主观题
网址:http://m.1010jiajiao.com/timu3_id_349033[举报]
在地壳内,深度每增加1km,压强大约增加25 250kPa~30 300kPa,在这样的压强下,对固体物质的平衡会发生较大影响.如:
|
查看习题详情和答案>>
(附加题)海水中化学资源的综合开发利用,已受到各国的高度重视.Br2和Mg等两种单质都可以从海水中提取,下图为提取它们的主要步骤:
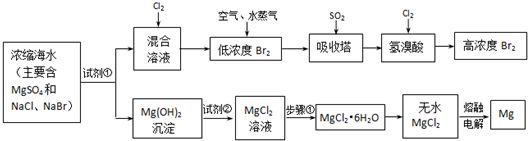
请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的1/3,主要方法就是上述流程中的空气吹出法.
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是
(2)吸收塔中反应的离子方程式是
由(1)、(2)可知,SO2、Cl2、Br2 三种物质氧化性由强到弱的顺序是
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的.
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用
(2)加入试剂②后反应的离子方程式是
(3)步骤①包括加热、蒸发、冷却、结晶、
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
Ⅲ.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸.生产方法是:
①将氯化镁晶体(MgCl2?6H2O)加热到523℃以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体.
②将两种气体冷却至室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸.
(1)MgCl2?6H2O在523℃以上分解的化学方程式是
(2)现用1mol MgCl2?6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水
查看习题详情和答案>>

请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的1/3,主要方法就是上述流程中的空气吹出法.
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是
Cl2+2Br-═2Cl-+Br2
Cl2+2Br-═2Cl-+Br2
.(2)吸收塔中反应的离子方程式是
Br2+SO2+2H2O═4H++SO42-+2Br-
Br2+SO2+2H2O═4H++SO42-+2Br-
.由(1)、(2)可知,SO2、Cl2、Br2 三种物质氧化性由强到弱的顺序是
Cl2>Br2>SO2
Cl2>Br2>SO2
.(用“>”表示)Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的.
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用
NaOH
NaOH
(写化学式).(2)加入试剂②后反应的离子方程式是
Mg(OH)2+2H+═Mg2++2H2O
Mg(OH)2+2H+═Mg2++2H2O
.(3)步骤①包括加热、蒸发、冷却、结晶、
过滤
过滤
.(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
MgCl2(熔融)
Mg+Cl2↑
| ||
MgCl2(熔融)
Mg+Cl2↑
.
| ||
Ⅲ.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸.生产方法是:
①将氯化镁晶体(MgCl2?6H2O)加热到523℃以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体.
②将两种气体冷却至室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸.
(1)MgCl2?6H2O在523℃以上分解的化学方程式是
MgCl2?6H2O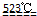 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑
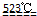 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑MgCl2?6H2O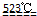 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑
.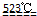 MgO+2 HCl↑+5H2O↑
MgO+2 HCl↑+5H2O↑(2)现用1mol MgCl2?6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水
36.9 g
36.9 g
g(精确到0.1),该盐酸中溶质的物质的量浓度是11.9
11.9
mol/L(精确到0.1).
硅是带来人类文明的重要元素之一.硅及其化合物在材料、电子信息等方面具有重要运用.回答下列问题:
(1)将下列硅酸盐改写成氧化物的形式(改写时注意金属氧化物在前.非金属氧化物在后,低价在前,高价在后,H2O一般写在最后).
①镁橄榄石(Mg2SiO4): .
②高岭土[Al2(Si2O3)(OH)4]: .
(2)玻璃是硅酸盐,工业上用石灰石、纯碱、石英在玻璃熔炉中熔融制得,写出相应的化学方程式 , .实验室盛放烧碱溶液的试剂瓶的瓶塞不能用玻璃塞,而用橡皮塞.其原因为(用化学方程式表示) .
(3)工业上用碳在高温下与二氧化硅制取粗硅,写出该反应的方程式 .
查看习题详情和答案>>
(1)将下列硅酸盐改写成氧化物的形式(改写时注意金属氧化物在前.非金属氧化物在后,低价在前,高价在后,H2O一般写在最后).
①镁橄榄石(Mg2SiO4):
②高岭土[Al2(Si2O3)(OH)4]:
(2)玻璃是硅酸盐,工业上用石灰石、纯碱、石英在玻璃熔炉中熔融制得,写出相应的化学方程式
(3)工业上用碳在高温下与二氧化硅制取粗硅,写出该反应的方程式
(2010?江苏)以水氯镁石(主要成分为MgCl2?6H2O)为原料生产碱式碳酸镁的主要流程如下:

(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6mol?L-1,则溶液中c(Mg2+)=
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为
(3)高温煅烧碱式碳酸镁得到MgO.取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L,通过计算确定碱式碳酸镁的化学式.
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数
查看习题详情和答案>>

(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6mol?L-1,则溶液中c(Mg2+)=
2.0mol?L-1
2.0mol?L-1
.(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为
NH4Cl
NH4Cl
.(3)高温煅烧碱式碳酸镁得到MgO.取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L,通过计算确定碱式碳酸镁的化学式.
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数
升高
升高
(填“升高”、“降低”或“不变”).我国的探月工程正在有计划的进行着,最近发射的嫦娥二号卫星又圆满完成了多项科学任务。月球上的主要矿物有辉石[CaMgSi2O6]、斜长石[KAlSi3O8]和橄榄石(可分为铁橄榄石[Fe2SiO4]、镁橄榄石[Mg2SiO4]、铁-镁橄榄石[(Mg∙Fe)2SiO4])等。
(1)铁橄榄石中铁元素化合价为______,硅元素原子核外电子排布式为_____________。
(2)硅元素的原子核外共有______种不同能级的电子,其原子最外层共有_____种不同运动状态的电子。
(3)月球上的上述主要矿物中,属于短周期元素的原子半径由大到小依次为__________
(填相应的元素符号),在这些短周期元素中,其单质晶体微粒间存在两种相互作用的是_____元素。
(4)某元素与氧元素同周期,且与氧元素组成的化合物中氧元素显正+2价,写出一个化学方程式,说明该元素与氧元素的非金属性的强弱________________________。
查看习题详情和答案>>