摘要:3] C
网址:http://m.1010jiajiao.com/timu3_id_345511[举报]
C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质.D的最外层电子数是次外层电子数的3倍,C、G同周期,且最外层电子数相差4,它们的简单离子电子层结构不同.相互间有如下转化关系:
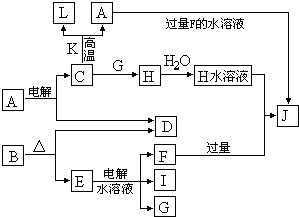
请填空:
(1)D与I能形成原子个数比为1:1的共价化合物,请写出其分子式:
G与I也能形成原子个数比为1:1的共价化合物,请写出其电子式: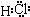
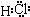 .
.
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解1L1mol?L-1的E水溶液的化学方程式:
(3)化合物K 中含有组成单质L的元素,且该元素的质量分数为70%.反应C→L的化学方程式是
(4)写出A+F→J的离子方程式:
查看习题详情和答案>>

请填空:
(1)D与I能形成原子个数比为1:1的共价化合物,请写出其分子式:
H2O2
H2O2
;G与I也能形成原子个数比为1:1的共价化合物,请写出其电子式:
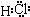
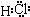
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解1L1mol?L-1的E水溶液的化学方程式:
2KCl+2H2O
2KOH+Cl2↑+H2↑
| ||
2KCl+2H2O
2KOH+Cl2↑+H2↑
,当溶液的pH=13时,理论上生成G的单质在标准状况下的体积为
| ||
1.12L
1.12L
;若将上述两电极材料调换,则阳极上的电极反应为Fe-2e-=Fe2+
Fe-2e-=Fe2+
.(3)化合物K 中含有组成单质L的元素,且该元素的质量分数为70%.反应C→L的化学方程式是
Fe2O3+2Al
Al2O3+2Fe
| ||
Fe2O3+2Al
Al2O3+2Fe
| ||
(4)写出A+F→J的离子方程式:
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.3月11日的日本大地震使福岛第一核电站受损,泄漏放射性物质131I、132I、和134Cs、137Cs等导致核污染.服用一定剂量的碘片可防放射性碘的伤害.下列说法错误的是( )
查看习题详情和答案>>
3月22日是世界水日,今年世界水日的主题是“涉水卫生”.混凝法是净化水常用的方法,在天然水或污水中加入一定的混凝剂,可使水中的悬浮物变为沉淀而除去.下列物质中不可以作为混凝剂的是( )
查看习题详情和答案>>
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用.请回答下列问题:
(1)32号元素Ge的原子核外电子排布式为
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3)已知SnO2是离子晶体,写出其主要物理性质
(4)已知:
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是
结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时
查看习题详情和答案>>
(1)32号元素Ge的原子核外电子排布式为
[Ar]3d104s24p2
[Ar]3d104s24p2
.(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
Sn
Sn
.(3)已知SnO2是离子晶体,写出其主要物理性质
熔沸点较高,硬度较大
熔沸点较高,硬度较大
(写出2条即可).(4)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是
CH4和SiH4比较,相对分子质量越大,范德华力越大,故沸点高,而NH3和PH3比较前者分子间存在氢键沸点高
CH4和SiH4比较,相对分子质量越大,范德华力越大,故沸点高,而NH3和PH3比较前者分子间存在氢键沸点高
.②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是
分解破坏的均为共价键,C-H的键能大于Si-H的键能,N-H键的键能大于P-H键的键能
分解破坏的均为共价键,C-H的键能大于Si-H的键能,N-H键的键能大于P-H键的键能
.结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时
HF
HF
先液化.C和Si元素在化学中占有极其重要的地位.
(1)写出Si的基态原子核外电子排布式
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为
(3)氧化物MO的电子总数与SiC的相等,则M为
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π健.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π健
(5)有A、B、C三种物质,每个分子中都各有14个电子,其中A的分子属于非极性分子,且只有非极性键;B的分子也属于非极性分子,但既有非极性键,又有极性键;C的分子属于极性分子.则可推出:A的电子式是
 ,B的结构式是
,B的结构式是
(6)已知Si-Si键能为176kJ/mol,Si-O键能为460kJ/mol,O=O键能为497.3kJ/mol.则可计算出1mol硅与足量氧气反应时将放出
查看习题详情和答案>>
(1)写出Si的基态原子核外电子排布式
1s22s22p63s23p2
1s22s22p63s23p2
.从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为O>C>Si
O>C>Si
.(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为
sp3
sp3
,微粒间存在的作用力是共价键
共价键
.(3)氧化物MO的电子总数与SiC的相等,则M为
Mg
Mg
(填元素符号),MO是优良的耐高温材料,其晶体结构与NaCl晶体相似,MO的熔点比CaO的高,其原因是Ca2+的离子半径大于Mg2+,MgO的晶格能大
Ca2+的离子半径大于Mg2+,MgO的晶格能大
.(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π健.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π健
Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不能形成上述稳定的π键
Si、O原子间距离较大,p-p轨道肩并肩重叠程度较小,不能形成上述稳定的π键
.(5)有A、B、C三种物质,每个分子中都各有14个电子,其中A的分子属于非极性分子,且只有非极性键;B的分子也属于非极性分子,但既有非极性键,又有极性键;C的分子属于极性分子.则可推出:A的电子式是


H-C≡C-H
H-C≡C-H
.(6)已知Si-Si键能为176kJ/mol,Si-O键能为460kJ/mol,O=O键能为497.3kJ/mol.则可计算出1mol硅与足量氧气反应时将放出
=-990.7
=-990.7
kJ的热量.