网址:http://m.1010jiajiao.com/timu3_id_340988[举报]
(1)钠与水的反应实验过程:将钠用________从煤油中取出,用________吸干煤油,然后在________上将钠用________切下块(选填“大”或“小”),投入盛有50mL水的锥形瓶中,充分反应后,滴人3滴酚酞。
反应原理:________。

注意事项:取钠块不要太大,否则易发生爆炸。不要用东西盖住锥形瓶,也不要用火点燃锥形瓶中的气体。
实验现象;①________,
②________,
③________,
④________。

实验结论:金属钠跟水反应的条件是_________;反应剧烈程度________;生成物的碱性________。
(2)镁与水的反应实验过程:①②③④反应原理:________。
注意事项:要用砂布除尽镁条表面的氧化膜,此反应需要加热或用热水。
实验现象:________实验结论:金属镁跟水反应的条件是________。反应剧烈程度________,生成物的碱性________

(3)铝与水的反应实验过程:①②③④反应原理:________注意事项:要除尽铝片表面的氧化膜。若用氢氧化钠溶液除表面的氧化膜,除后必须用清水把表面溶液洗净。此反应需加热或用热水。
实验现象:________实验结论:金属铝跟水反应的条件是________,反应剧烈程度________,生成物的碱性________。
查看习题详情和答案>>
钠、镁、铝等金属单质与水反应的情况
(1)钠与水的反应实验过程:将钠用________从煤油中取出,用________吸干煤油,然后在________上将钠用________切下块(选填“大”或“小”),投入盛有50mL水的锥形瓶中,充分反应后,滴人3滴酚酞。
反应原理:________。

注意事项:取钠块不要太大,否则易发生爆炸。不要用东西盖住锥形瓶,也不要用火点燃锥形瓶中的气体。
实验现象;①________,
②________,
③________,
④________。

实验结论:金属钠跟水反应的条件是_________;反应剧烈程度________;生成物的碱性________。
(2)镁与水的反应实验过程:①②③④反应原理:________。
注意事项:要用砂布除尽镁条表面的氧化膜,此反应需要加热或用热水。
实验现象:________实验结论:金属镁跟水反应的条件是________。反应剧烈程度________,生成物的碱性________

(3)铝与水的反应实验过程:①②③④反应原理:________注意事项:要除尽铝片表面的氧化膜。若用氢氧化钠溶液除表面的氧化膜,除后必须用清水把表面溶液洗净。此反应需加热或用热水。
实验现象:________实验结论:金属铝跟水反应的条件是________,反应剧烈程度________,生成物的碱性________。
查看习题详情和答案>>
①给盛有液体的烧瓶加热时,需要加碎瓷片或沸石
②用H2还原CuO时应先通H2再点燃酒精灯
③点燃可燃性气体前要验纯
④稀释浓硫酸时,要将浓硫酸慢慢沿器壁流入水中.

(1)写出上述流程中X物质的分子式
(2)使原料氯化钠的利用率从70%提高到90%以上,主要涉及了
(3)该实验得到的纯碱中含有氯化钠,甲同学设计如图3装置Ⅰ,拟通过测定烧杯中氢氧化钠溶液的增重来测定样品中碳酸钠的含量,但该实验存在明显不足,试举出该装置引起误差的两个主要原因:
①
②
(4)乙同学设计的测定样品中纯碱含量的方法如图3Ⅱ,试回答:
①检查该装置气密性的方法为:
②设滴定管的起始读数为V1mL,终了读数为V2mL,注射器收集的气体为V3mL(标准状况),称得样品质量为m g,则原样品中碳酸钠的质量分数的表达式为
| V3-(V2-V1) |
| 22400m |
| V3-(V2-V1) |
| 22400m |
(5)丙同学设计的测定样品中纯碱含量的方法如图3Ⅲ,并在广口瓶中的水上面滴加少量植物油,试回答:
①你认为植物油的作用是
②为减小误差,读取量筒中水的体积时的注意事项有:
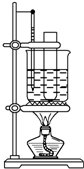 实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:
实验室制备硝基苯的方法是苯与浓硫酸和浓硝酸的混合液加热到55℃~60℃反应,已知苯与硝基苯的基本物理性质如下表所示:| 熔点 | 沸点 | 状态 | |
| 苯 | 5.51℃ | 80.1℃ | 液体 |
| 硝基苯 | 5.7℃ | 210.9℃ | 液体 |
(2)分离硝基苯和水的混合物的方法是
(3)某同学用如图装置制取硝基苯:
①用水浴加热的优点是
②指出该装置的两处缺陷