网址:http://m.1010jiajiao.com/timu3_id_340772[举报]
请回答下列问题:
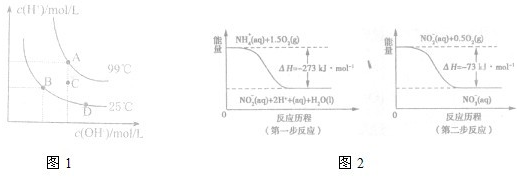
(1)已知水的电离平衡曲线如图1所示.A、B、C三点水的电离平衡常数KA、KB、KC关系为
a.加入少量盐酸
b.加入少量碳酸钠
c.加入少量氢氧化钠
d.降低温度
(2)饮用水中的NO3-主要来自于NH4+.已知在微生物的作用下,NH4+经过两步反应被氧化成NO3-.两步反应的能量变化如图2,1molNH4+全部被氧化成NO3-的热化学方程式为
(3)某工厂用电解法除去废水中含有的Cr2O72-,总反应方程式为:Cr2O72-+6Fe+17H2O+2H+ 2Cr(OH)3↓+6Fe(OH)3↓+6H2↑,该电解反应的负极材料反应的电极式为
(4)废水中的N、P元素是造成水体富营养化的主要因素,农药厂排放的废水中.常含有较多的NH4+和PO43-,其中一种方法是:在废水中加入镁矿工业废水,可以生成高品位的磷矿石--鸟粪石,反应的离子方程式为Mg2++NH4++PO43-→MgNH4PO4↓.该方法中需要控制污水的pH为7.5-10,若pH高于l0.7,鸟粪石产量会降低,其原因可能是
(8分)我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。根据你所学的知识,试回答下列问题:
(1)大气污染物二氧化硫溶于水生成亚硫酸,亚硫酸具有还原性,试写出雨水中亚硫酸被氧化为硫酸的化学方程式__________________________。
(2)某市是受酸雨影响比较严重的城市,电厂每年就要排放二氧化硫9.14万吨。目前该厂应用了国际上最成熟的石灰石-石膏湿法脱硫技术,使每年产生的二氧化硫成倍减少,“变”酸雨为石膏,达到了变废为宝的目的。请写出其中发生的反应中属于分解反应和化合反应的化学方程式各一个。
____________________________________________ 、 ____________________________________________。
(3)结合你所学的化学知识,你认为减少酸雨产生的途径还可采用的措施是___________________________________________________________。
查看习题详情和答案>>

请根据表回答下列问题:
(1)硒的熔点范围可能是_____________。
(2)碲的化合价可能有_____________。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱顺序是_____________(填化学式)。
(4)氢硒酸有较强的(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生的化学方程式为____________________________________。
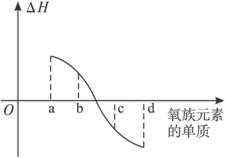
(5)下图所示为氧族元素单质与H2反应过程中的能量变化(ΔH)示意图,其中a、b、c、d分别表示氧族中某一元素的单质,ΔH为相同物质的量的单质与H2反应的反应热。则:b代表___________(写单质名称)。
(6)硫的最高价含氧酸(H2SO4)是一种用途广泛的化学试剂。工业大量生产时通常要经过①含硫物质的氧化 ②SO2催化氧化成SO3 ③SO3的吸收三个主要过程。已知SO2的催化氧化是一个放热的可逆反应,该反应化学平衡常数(K)的表达式为_______________________,为提高SO2的转化率,试写出两种可以采用的措施:_____________________________;_______________________________。吸收SO3时若反应过快会形成酸雾,则是否可以用水直接吸收?________________________。
查看习题详情和答案>>水是宝贵资源,研究生活和工业用水的处理有重要意义。请回答下列问题:
(1)已知水的电离平衡曲线如图所示。A、B、C三点水的电离平衡常数KA、KB、KC关系为 ,若从B点到D点,可采用的措施是 (填序号)。

a。加入少量盐酸
b.加人少量碳酸钠
c.加人少量氢氧化钠
d.降低温度
(2)饮用水中的NO3-主要来自于NH4+。已知在微生物的作用下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

1 molNH4+全部被氧化成NO3-的热化学方程式为 。
(3)某工厂用电解法除去废水中含有的Cr2O72-,总反应方程式为:
Cr2O72-+6Fe+17H2O+2H+
2Cr(OH)3↓+6Fe(OH)3 ↓+6H2↑,该电解反应的负极材料反应的电极式为
,若有9 mol电子发生转移,则生成的cr(OH)3物质的量为
。
(4)废水中的N、P元素是造成水体富营养化的主要因素,农药厂排放的废水中。常含有较多的NH4+和PO43-,其中一种方法是:在废水中加人镁矿工业废水,可以生成高品位的磷矿石——鸟粪石,反应的离子方程式为Mg2++NH4++PO43-
MgNH4PO4↓。该方法中需要控制污水的pH为7.5—10,若pH高于l0.7,鸟粪石产量会降;低,其原因可能是
。
查看习题详情和答案>>
(8分)我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。根据你所学的知识,试回答下列问题:
(1)大气污染物二氧化硫溶于水生成亚硫酸,亚硫酸具有还原性,试写出雨水中亚硫酸被氧化为硫酸的化学方程式__________________________。
(2)某市是受酸雨影响比较严重的城市,电厂每年就要排放二氧化硫9.14万吨。目前该厂应用了国际上最成熟的石灰石-石膏湿法脱硫技术,使每年产生的二氧化硫成倍减少,“变”酸雨为石膏,达到了变废为宝的目的。请写出其中发生的反应中属于分解反应和化合反应的化学方程式各一个。
____________________________________________ 、 ____________________________________________。
(3)结合你所学的化学知识,你认为减少酸雨产生的途径还可采用的措施是___________________________________________________________。
查看习题详情和答案>>