网址:http://m.1010jiajiao.com/timu3_id_338519[举报]
下列几种物质中互为同分异构体的是( )
A.水和重水 B. 氧气和臭氧 C. 2—甲基丁烷和新戊烷 D.氘和氚
【解析】分子式相同而结构不同的化合物互称为同分异构体。质子数相同而质量数不同的核素互称为同位素。由同一种元素形成的不同单质互称为同素异形体。水和重水都表示水分子,化学性质几乎是相同的,不属于同分异构体。氧气和臭氧属于同素异形体,氘和氚属于同位素。所以正确的答案是C。
查看习题详情和答案>>
下列几种物质中互为同分异构体的是( )
A.水和重水 B. 氧气和臭氧 C. 2—甲基丁烷和新戊烷 D.氘和氚
【解析】分子式相同而结构不同的化合物互称为同分异构体。质子数相同而质量数不同的核素互称为同位素。由同一种元素形成的不同单质互称为同素异形体。水和重水都表示水分子,化学性质几乎是相同的,不属于同分异构体。氧气和臭氧属于同素异形体,氘和氚属于同位素。所以正确的答案是C。
查看习题详情和答案>>
(8分)1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子。O3的分子结构如下,请回答:
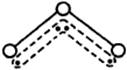 |
⑴ 题中非极性共价键是 键,特殊的化学键是 键。(填“σ”或“π”)
⑵ 人们在研究分子结构时总结出一条经验规律:具有相同价电子数和相同 原子数的分子或离子具有相同的结构特征,这一原理称为“等电子原理”。下列物质的分子与O3分子的结构最相似的是 。
A.H2O B.CO2 C.SO2 D.BeCl2
⑶ 原子中没有跟其他原子共用的电子对叫孤对电子,那么O3分子有 对孤对电子。
![]() ⑷ 下列有关说法中正确的是 。
⑷ 下列有关说法中正确的是 。
A.臭氧和氧气互为同素异形体,它们在水中的溶解度相近
B.臭氧和氧气的相互转化能保持大气中臭氧的含量基本稳定
C.臭氧转化为氧气和氧气转化为臭氧均需吸收能量
D.向大气中排放氟氯代烃能加快臭氧的分解
查看习题详情和答案>>