摘要:38.4 g Cu跟适量的HNO3作用.铜全部反应后.共收集到气体22.4 L.反应消耗的硝酸的物质的量可能是( ) A.1 mol B.2.2 mol C.1.6 mol D.2.4 mol
网址:http://m.1010jiajiao.com/timu3_id_338380[举报]
38.4 g Cu跟适量的HNO3作用,铜全部反应后,共收集到气体22.4 L(标准状况),反应消耗的硝酸的物质的量可能是( )
A.1 mol B.2.2 mol C.1.6 mol D.2.4 mol
查看习题详情和答案>>
设NA代表阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,17 g氨气所占体积小于22.4 L
B. 3 mol NO2与水反应转移(偏移)电子数为3NA
C.标准状况下22.4 L的氮气所含的原子数为NA
D.6.4 g Cu片跟浓、稀HNO3完全反应,失电子数都为0.2NA
查看习题详情和答案>>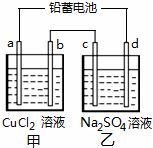 (2010?丰台区二模)用铅蓄电池电解甲、乙电解池中的溶液.已知铅蓄电池的总反应为:
(2010?丰台区二模)用铅蓄电池电解甲、乙电解池中的溶液.已知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq)
| 放电 |
| 充电 |
电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )
查看习题详情和答案>>
在25℃时,用石墨电极电解2.0 L,2.5mol/LCuSO4溶液.5min后,在一个石墨电极上有6.4 g Cu生成.试回答下列问题:
(1)
(2)
(3)有
(4)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差
查看习题详情和答案>>
(1)
阳
阳
极发生氧化反应(填阴,阳),电极反应式为4OH--4e-═2H2O+O2↑
4OH--4e-═2H2O+O2↑
.(2)
阴
阴
极发生还原反应(填阴,阳),电极反应式为2Cu2++4e-═2Cu
2Cu2++4e-═2Cu
.(3)有
0.2
0.2
mol电子发生转移,得到氧气的体积(标准状况)是1.12
1.12
L,溶液的pH是1
1
.反应速率v(Cu2+):v(O2)═2:1
2:1
(4)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差
12.8
12.8
g,电解液的pH不变
不变
(填“变小”、“变大”或“不变”)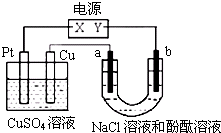 如图,a、b是石墨电极,通电一段时间后,a极附近溶液显红色.下列说法不正确的是( )
如图,a、b是石墨电极,通电一段时间后,a极附近溶液显红色.下列说法不正确的是( )