网址:http://m.1010jiajiao.com/timu3_id_337132[举报]

(1)写出装置丁中发生的化学反应方程式:_____________________。
(2)证明氯水已饱和的现象是________________。
(3)制取结束时,装置丙中的液体含有的微粒是________________(用微粒符号表示);
(4)测定饱和氯水的pH方法是____。若撤去装置乙,直接将装置甲和丙相连。这样做对实验测定结果的影响是____________________。
(5)饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一。如图所示:

Ⅱ过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强。
Ⅲ为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2气体。
①能用饱和氯水与石灰石反应制备较浓HClO溶液的原因是____。
②依据上述实验可推知,Ⅱ的滤液中的溶质除CaCl2、HClO和极少量的氯气外,还含有_____________(写化学式)。
③写出步骤Ⅲ中,第二份滤液发生的离子反应方程式:____________________。

(1)实验步骤的顺序应为(填序号)________________________。
(2)用a、b、c表示的钠的相对原子质量为________________________。
(3)下列因素对实验结果分别有何影响(填“偏大”或“偏小”)?
①没有B装置:_________________________________________。
②用金属钠时未吸干煤油:__________________。
③称得的金属钠表面变暗后才放入锥形瓶_________________________________。
④反应时,钠燃烧起来:_________________________。
查看习题详情和答案>>
请根据题意回答下列问题:
(1)实验步骤的顺序应为(填序号)____________。
(2)用a、b、c表示钠的相对原子质量为______________________________。
(3)下列因素对实验结果分别有何影响?(填“偏大”“偏小”或“无影响”)①没有B装置__________;②取用金属钠时未吸干煤油__________;③称得的金属钠表面变暗后才放入锥形瓶_______________;④反应时,钠燃烧起来________________。
查看习题详情和答案>>为测定钠的相对原子质量,某同学设计了如图2-3所示的反应装置,现有如下步骤:①称量A、B的总质量 ②称取一定质量的钠 ③将钠投入锥形瓶中并迅速塞紧带U形干燥管的橡皮塞 ④用镊子取金属钠并用滤纸吸干煤油。有关数据是:称取的金属钠质量为a g,A、B反应前总质量为b g,反应后A、B的总质量为c g。请根据题意完成下列问题:

图2-3
(1)实验步骤的顺序应为(填序号) 。
(2)用a、b、c表示的钠的相对原子质量为 。
(3)下列因素对实验结果分别有何影响(填“偏大”或“偏小”)?
①没有B装置: 。
②用金属钠时未吸干煤油: 。
③称得的金属钠表面变暗后才放入锥形瓶: 。
④反应时,钠燃烧起来: 。
查看习题详情和答案>>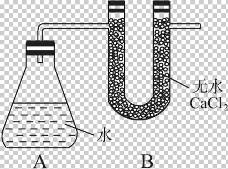
图2-3
(1)实验步骤的顺序应为(填序号) 。
(2)用a、b、c表示的钠的相对原子质量为 。
(3)下列因素对实验结果分别有何影响(填“偏大”或“偏小”)?
①没有B装置: 。
②用金属钠时未吸干煤油: 。
③称得的金属钠表面变暗后才放入锥形瓶: 。
④反应时,钠燃烧起来: 。