摘要:在重铬酸钾(K2Cr2O7)溶液中存在如下平衡: Cr2O2-7+H202HCrO-7 Cr2O2-4+2H+ (1)加入H2SO4.使Cr2O72-溶液的pH降低.则溶液中c(Cr2O72-)与c(Cr2O42-)的比值 将 (填“增大 .“减小 或“不变 ). (2)向K2Cr2O7溶液中加入AgNO3溶液.发生离子互换反应.生成砖红色沉淀且溶液的pH下降.生成的砖红色沉淀的化学式为 . (3)重铬酸钾在酸性溶液中是强氧化剂.例如它在H2SO4存在的条件下要把Fe2+离子 氧化成Fe3+离子.本身被还原成Cr3+离子.该反应的离子方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_335788[举报]
在重铬酸钾(K2Cr2O7)溶液中存在如下平衡: Cr2O72-+H2O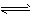 2HCrO4-
2HCrO4- 2H++2CrO42- ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
2H++2CrO42- ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
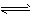 2HCrO4-
2HCrO4- 2H++2CrO42- ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
2H++2CrO42- ,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为 [ ]
A. Ag2Cr2O7
B. Ag2CrO4
C. AgHCrO4
D. Ag2O
查看习题详情和答案>>
B. Ag2CrO4
C. AgHCrO4
D. Ag2O
在重铬酸钾(K2Cr2O7)溶液中存在如下平衡:CrO
+H2O?2HCrO
?2H++2CrO
,向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为( )
2- 7 |
- 4 |
2- 4 |
查看习题详情和答案>>
在重铬酸钾(K2Cr2O7)溶液中存在如下平衡:
Cr2O72-+H2O ![]() 2HcrO4
2HcrO4 ![]() 2CrO42-+2H+
2CrO42-+2H+
(1)加入H2SO4,使K2Cr2O7溶液的pH降低,则溶液中c(Cr2O72-)与c(CrO42-)的比值将 (填“增大”“减小”或“不变”)
(2)向K2Cr2O7溶液中加入AgNO3溶液,发生离子互换反应,生成砖红色沉淀且溶液的pH下降,生成的砖红色沉淀的化学式为 。
(3)重铬酸钾在酸性溶液中是强氧化剂。例如它在H2SO4存在的条件下要把Fe2+离子氧化成Fe3+离子,本身被还原成Cr3+离子。该反应的离子方程式为 。
查看习题详情和答案>>在重铬酸钾(K2Cr2O7)溶液中存在如下平衡: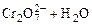

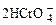

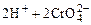 , 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
, 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
| A.Ag2O | B.Ag2CrO4 | C.AgHCrO4 | D.Ag2Cr2O7 |



 , 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
, 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为