摘要:用铅蓄电池作电源时,正极材料是PbO2,负极材料是Pb,其放电过程可以表示为:Pb+PbO2+2H2SO4===2PbSO4+2H2O充电时发生还原反应的电极方程式为 ( ) A.Pb-2e-===Pb2+ C.PbO2+4H++2e- ===Pb2++2H2O D.PbSO4+2e- ===Pb+SO42-
网址:http://m.1010jiajiao.com/timu3_id_335195[举报]
铅蓄电池作电源时,正极材料是PbO2,负极材料是Pb,内充稀硫酸,两极总反应为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
A.PbO2+4H++2e-![]() Pb2++2H2O
Pb2++2H2O
B.Pb-2e-![]() Pb2+
Pb2+
C.PbSO4+2e-![]() Pb+SO
Pb+SO![]()
D.PbSO4+2H+-2e-![]() PbO2+4H++SO
PbO2+4H++SO![]()
铅蓄电池作电源时,正极材料是PbO2,负极材料是Pb,内充稀硫酸,两极总反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
 2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )A.PbO2+4H++2e- Pb2++2H2O Pb2++2H2O |
B.Pb-2e- Pb2+ Pb2+ |
C.PbSO4+2e- Pb+SO Pb+SO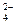 |
D.PbSO4+2H+-2e- PbO2+4H++SO PbO2+4H++SO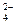 |
铅蓄电池是化学电源,它工作时的电池反应为:PbO2+Pb+2H2SO4═2PbSO4+2H2O.
试回答:
(1)铅蓄电池正极的电极材料是
(2)工作时该铅蓄电池负极的电极反应是
(3)铅蓄电池工作时,电解质溶液的密度
(4)如果用铅蓄电池做电源电解饱和食盐水制取Cl2,当制得0.05mol Cl2时,在理论上电池内部消耗的H2SO4的物质的量是
查看习题详情和答案>>
试回答:
(1)铅蓄电池正极的电极材料是
PbO2
PbO2
.(2)工作时该铅蓄电池负极的电极反应是
Pb+SO42--2e-═PbSO4
Pb+SO42--2e-═PbSO4
.(3)铅蓄电池工作时,电解质溶液的密度
减小
减小
(填“减小”“增大”或“不变”,下同),pH增大
增大
.(4)如果用铅蓄电池做电源电解饱和食盐水制取Cl2,当制得0.05mol Cl2时,在理论上电池内部消耗的H2SO4的物质的量是
0.1mol
0.1mol
.