网址:http://m.1010jiajiao.com/timu3_id_334597[举报]

(2)元素甲是第三周期ⅦA族元素,化合物A是由甲元素等非金属元素组成的离子化合物写出其化学式
(3)元素乙是第三周期原子半径最小的金属元素,丙是短周期元素中原子半径最大的元素,用电子式表示丙在空气中加热反应生成B的形成过程


(4)化合物C是由甲元素和乙元素形成的化合物,将化合物A与化合物C等物质的量溶于水中,向其中滴加过量的2mol?L-1氢氧化钠溶液,直至形成透明溶液.请根据实验现象出现的先后顺序,依次写出离子方程式:
(5)实验中丙元素的鉴别方法
| 结构简式 |  |
 |
 |
| 键线式 |  |
 |
 |
(2)
 的分子式为
的分子式为(3)乙炔3分子聚合的产物为苯.写出丙炔三分子聚合形成的芳香烃分子的键线式


(4)由
 以及必要的无机试剂可合成
以及必要的无机试剂可合成 ,写出第一步合成反应的化学方程式
,写出第一步合成反应的化学方程式

(5)
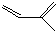 的一种同分异构体A,它的一氯代物有三种.与Br2按1:1加成产物只有一种(不考虑顺反、立体异构),则A的结构简式为
的一种同分异构体A,它的一氯代物有三种.与Br2按1:1加成产物只有一种(不考虑顺反、立体异构),则A的结构简式为

Ⅱ乙基香草醛(
 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.(1)乙基香草醛分子中的含氧官能团有乙氧基、
乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:

提示:a.RCH2OH
| CrO3/H2SO4 |
b.与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基.
(2)A生成C的反应类型是
(3)写出在加热条件下C与NaOH水溶液发生反应的化学方程式


(4)乙基香草醛的另一种同分异构体D(
 )是一种医药中间体.
)是一种医药中间体.请设计合理方案用茴香醛(
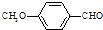 )合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭号下方,试剂或原料写在箭号上方,中间产物填在下图中的方框内.并写出茴香醛与银氨溶液反应的化学方程式.
)合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭号下方,试剂或原料写在箭号上方,中间产物填在下图中的方框内.并写出茴香醛与银氨溶液反应的化学方程式.




(8分)在加热条件下发生某一化学反应,现对反应体系内的X、Y、Z、Q四种物质是行测定,测得如下数据:
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量/g | 43.6 | 待测数据 | 12.6 | 3.2[来源:Z|xx|k.Com] |
(1)上表中“等测数据”的数值是 ,此密闭容器中化学反应类型属于 反应(填基本反应类型)。
(2)若X是水,Y是氮的氧化物,且反应式的计量系数比n(X):n(Y):n(Z):n(Q)=2:4:4:1,写出化学反应的方程式: 。
(3)反应结束后,若将反应体系内的Y物质取出,要标准状况下测得其体积小于11.2L,其原因是 。 查看习题详情和答案>>
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00 mL密度为ρ g/mL的过氧化氢溶液稀释至250mL。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样。此过程中需要用到的定量仪器 。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程:___MnO4- + __H2O2 + ___H+ → ___Mn2+ + __H2O +__ _____
(3) 滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是_____________________ ___。
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为___________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____(填“偏高”“偏低”“不变”)。
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、二氧化锰,实验仪器及用品可自选。)
请将他们所选的实验试剂和实验现象填入下表:(只要完成其中一项探究即可)
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 |
|
|
| 或探究不稳定性 |
|
|
查看习题详情和答案>>
图一是煤化工产业链的一部分,试运用所学知识,回答下列问题:
图一
(1)图一中气体A的俗称是_______________
(2)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1mol氮气中的化学键需要吸收946 kJ能量;破坏0.5mol氢气中的H-H键需要吸收218kJ的能量;形成氨分子中1 mol N-H键能够释放389kJ能量。图二表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值,填在下边的横线上。 
图二
① kJ ,② kJ
(3)煤化工产业的重要产品之一甲醇,是一种新型的汽车动力燃料,发达国家等一般通过CO和H2化合制备甲醇,该反应的化学方程式为:CO (g) + 2H2(g) CH3OH(g)
CH3OH(g)
①下列描述中能说明上述反应已达平衡的是_______;
A. 容器内气体的平均摩尔质量保持不变
B. 2v(H2)正 = v(CH3OH)逆
C. 容器中气体的压强保持不变
D. 单位时间内生成n molCO的同时生成2n mol H2
②在容积固定的恒温密闭容器中充入CO和H2发生上述反应,反应在第4 min时候达到其限度,此时容器中压强与反应前之比为3︰5,容器内物质的各种物质的量浓度如下表:
| 时间/浓度 | c(CO)(mol/L) | C(H2 )(mol/L) | c(CH3OH)(mol/L) |
| 起始 | 0.200 | 0.300 | 0.000 |
| 第4 min | a | b | c |
(4)甲醇—空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,其工作原理如下图所示,该燃料电池的电池反应式为2CH3OH (g) + 3O2(g) = 2CO2(g) + 4H2O(l),则负极的电极反应式为______________________,正极附近pH值_______________(填写“增大”、“减小”或者“不变”)
 查看习题详情和答案>>
查看习题详情和答案>>