摘要:一定条件下,将W克的氢气或一氧化碳或是二者的混合气体,在足量的氧气中充分燃烧后,将生成的气体通过足量的过氧化钠后,过氧化钠的质量增加W克,由些分析得出只要其化学组成符合 的物质,在足量的氧气中充分燃烧后,将生成的气体通过足量的过氧化钠时其增加质量就等于原来物质的质量.符合上述组成的某种有机物0.1mol在氧气中充分燃烧后生成CO2和H2O水均为0.2mol.并放出akJ热量.则在通常状 态下该物质燃烧的热化学方程是 . 符合上述组成的有机物可能的结构简式有
网址:http://m.1010jiajiao.com/timu3_id_331480[举报]
(2011?新余二模)X、Y都是芳香族化合物,均为常见食用香精,广泛用于化妆品、糖果及调味品中.1mol X水解得到1mol Y和1mol CH3CH2OH,X、Y的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且X分子中碳和氢元素总的质量百分含量约为 81.8%.
(1)X、Y相对分子质量之差为
(2)1个Y分子中应该有
(3)X的分子式是
(4)G和X互为同分异构体,且具有相同的官能团,用芳香烃A合成G路线如下:

①写出A的结构简式

②E→F的反应类型是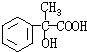
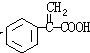 +H2O
+H2O
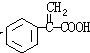 +H2O
+H2O
③写出所有符合下列条件的F的同分异构体的结构简式: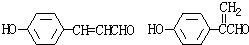
 .
.
i.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基.
ii.一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应.
查看习题详情和答案>>
(1)X、Y相对分子质量之差为
28
28
.(2)1个Y分子中应该有
2
2
个氧原子.(3)X的分子式是
C11H12O2
C11H12O2
(4)G和X互为同分异构体,且具有相同的官能团,用芳香烃A合成G路线如下:

①写出A的结构简式


②E→F的反应类型是
消去
消去
反应,该反应的化学方程式为:
| 浓硫酸 |
| △ |
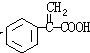 +H2O
+H2O
| 浓硫酸 |
| △ |
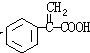 +H2O
+H2O③写出所有符合下列条件的F的同分异构体的结构简式:


i.分子内除了苯环无其他环状结构,且苯环上有2个对位取代基.
ii.一定条件下该物质既能与银氨溶液发生银镜反应又能和FeCl3溶液发生显色反应.
已知:
Ⅰ.
Ⅱ.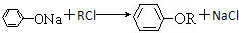
冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如图所示:
(1)A是饱和一元羧酸,8.8gA与足量NaHCO3溶液反应生成 2.24L(标准状况)CO2,则A的分子式为
(2)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B水解生成化合物G的反应方程式:
 .
.
(3)写出H→X的化学方程式: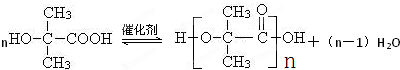
 .
.
(4)D的苯环上有两种氢,其结构简式是
 ,D具有的性质有
,D具有的性质有
A.可以发生消去反应、取代反应
B.可以发生加成反应、氧化反应
C.在一定条件下,与氢氧化钠反应,最多消耗2mol NaOH
D.能与FeCl3溶液发生显色反应
(5)写出C→F的化学方程式:
 .
.
(6)聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维.若用上述物质中的C通过2步反应合成高聚物Y( ),反应的化学方程式是:第一步:
),反应的化学方程式是:第一步:
 ;第二步:
;第二步:
 .
.
(7)与B互为同分异构体的属于酯类的化合物共有 结构).
结构).
查看习题详情和答案>>
Ⅰ.

Ⅱ.
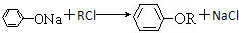
冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如图所示:

(1)A是饱和一元羧酸,8.8gA与足量NaHCO3溶液反应生成 2.24L(标准状况)CO2,则A的分子式为
C4H8O2
C4H8O2
.(2)B是氯代羧酸,其核磁共振氢谱有两个峰,写出B水解生成化合物G的反应方程式:


(3)写出H→X的化学方程式:


(4)D的苯环上有两种氢,其结构简式是


BD
BD
.A.可以发生消去反应、取代反应
B.可以发生加成反应、氧化反应
C.在一定条件下,与氢氧化钠反应,最多消耗2mol NaOH
D.能与FeCl3溶液发生显色反应
(5)写出C→F的化学方程式:


(6)聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维.若用上述物质中的C通过2步反应合成高聚物Y(
 ),反应的化学方程式是:第一步:
),反应的化学方程式是:第一步:



(7)与B互为同分异构体的属于酯类的化合物共有
11
11
种(不含 结构).
结构).
二甲醚是一种重要的清洁燃料,工业上可利用煤的气化产物(水煤气)合成二甲醚.利用水煤气合成二甲醚的热化学方程式为:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-274kJ?mol-1.
(1)该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是 (填字母)
A.降低温度 B.加入催化剂 C.缩小容器体积 D.增加H2的浓度 E.分离出二甲醚
(2)该反应可以分两步进行:
4H2(g)+2CO(g)═CH3OCH3(g)+H2O(g)△H1 ①
CO(g)+H2O(g)═CO2(g)+H2△H2=-42kJ?mol-1
则反应①的焓变△H1= kJ?mol-1,熵变△S (填“>、<或=”)0.
已知某些化学键的键能数据如下表所示:
CO中C与O之间为叁键连接,则CO2中碳氧键的键能是 kJ?mol-1.
(3)二甲醚也可以通过CH3OH分子间脱水制得:
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H3=-23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度变化如下表:
①该条件下反应平衡常数K= .
②相同条件下,若改变起始浓度.
此时正、逆反应速率的大小:v正 (填“>、<或=”)v逆.
(4)二甲醚-空气是一种高效的燃料电池,在氢氧化钾溶液中,电池反应方程式为:
CH3OCH3(l)+3O2(g)+4KOH(aq)═2K2CO3(aq)+5H2O(l)
请写出负极的电极反应式: .
查看习题详情和答案>>
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-274kJ?mol-1.
(1)该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是
A.降低温度 B.加入催化剂 C.缩小容器体积 D.增加H2的浓度 E.分离出二甲醚
(2)该反应可以分两步进行:
4H2(g)+2CO(g)═CH3OCH3(g)+H2O(g)△H1 ①
CO(g)+H2O(g)═CO2(g)+H2△H2=-42kJ?mol-1
则反应①的焓变△H1=
已知某些化学键的键能数据如下表所示:
| 化学键 | C-H | O-H | H-H | C-O | C≡O |
| 键能/kJ.mol-1 | 413 | 463 | 436 | 358 | 1072 |
(3)二甲醚也可以通过CH3OH分子间脱水制得:
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H3=-23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度变化如下表:
| 物质 | CH3OH (g) | CH3OCH3 (g) | H2O (g) |
| 起始浓度/mol.l-1 | 2 | 0.2 | 0 |
| 平衡浓度/mol.l-1 | 0.4 | 1 | 0.8 |
②相同条件下,若改变起始浓度.
| 物质 | CH3OH (g) | CH3OCH3 (g) | H2O (g) |
| 起始浓度/mol.l-1 | 0.4 | 1.2 | 0.6 |
(4)二甲醚-空气是一种高效的燃料电池,在氢氧化钾溶液中,电池反应方程式为:
CH3OCH3(l)+3O2(g)+4KOH(aq)═2K2CO3(aq)+5H2O(l)
请写出负极的电极反应式:
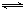 2SO3的化学平衡体系中,各物质的浓度分别是2.0mol/L、0.8mol/L、2.4mol/L,则氧气在反应起始时的浓度可能是( )
2SO3的化学平衡体系中,各物质的浓度分别是2.0mol/L、0.8mol/L、2.4mol/L,则氧气在反应起始时的浓度可能是( )