摘要:解:先把10℃时100克KNO3饱和溶液中含KNO3的质量x 121∶21 = 100克∶x 克 则: 100克KNO3饱和溶液中溶剂质量为 100克-17.3克 = 82.7克 升温后82.7克溶剂中可溶解KNO3质量为y. 100∶108 = 82.7克∶y 克 ∴还能溶解KNO3晶体:
网址:http://m.1010jiajiao.com/timu3_id_328811[举报]
下列各组溶液,同时开始反应,最先出现浑浊的一组是( )
A.10 ℃时5 mL 0.1 mol·L-1 Na2S2O3溶液与5 mL 0.1 mol·L-1 H2SO4溶液混合
B.10 ℃时10 mL 0.05 mol·L-1 Na2S2O3溶液与10 mL 0.1 mol·L-1 H2SO4溶液混合
C.20 ℃时5 mL 0.1 mol·L-1 Na2S2O3溶液与5 mL 0.1 mol·L-1 H2SO4溶液混合
D.20 ℃时5 mL 0.05 mol·L-1 Na2S2O3溶液与5 mL 0.05 mol·L-1 H2SO4溶液混合
查看习题详情和答案>>|
现有下列各组溶液:①10℃时10 mL 0.1 mol/L的Na2S2O3溶液和10 mL 0.1 mol/L的H2SO4溶液;②10℃时10 mL 0.05 mol/L的Na2S2O3溶液和l0 mL 0.1 mol/L的H2SO4溶液;③30℃时10 mL 0.1 mol/L的Na2S2O3溶液和10 mL 0.1 mol/L的H2SO4溶液.若同时将它们混合发生反应:Na2S2O3+H2SO4≒Na2SO4+S↓+SO2↑+H2O,则出现浑浊的先后次序是 | |
| [ ] | |
A. |
①②③ |
B. |
②①③ |
C. |
①③② |
D. |
③①② |
现有下列各组溶液:
①10℃时10 mL 0.1 mol/L的Na2S2O3溶液和10 mL 0.1 mol/L的H2SO4溶液;
②10℃时10 mL 0.05 mol/L的Na2S2O3溶液和l0 mL 0.1 mol/L的H2SO4溶液;
③30℃时10 mL 0.1 mol/L的Na2S2O3溶液和10 mL 0.1 mol/L的H2SO4溶液.若同时将它们混合发生反应:Na2S2O3+H2SO4≒Na2SO4+S↓+SO2↑+H2O,则出现浑浊的先后次序是
- A.①②③
- B.②①③
- C.①③②
- D.③①②
Ⅰ.菠菜是常见蔬菜,100g菠菜中含有的营养成分为:草酸0.2-0.3g,水91.2g,蛋白质2.6g,脂肪0.3g,纤维素1.7g,糖类2.8g,维生素B1 0.04mg,维生素B2 0.11mg,维生素C 32mg,维E 1.74mg,Fe 2.9mg,Se 0.97g,胡萝卜素2.92mg,视黄醇0.487mg等.
(1)菠菜中铁的主要存在价态是
(2)验证菠菜中草酸的存在要先把草酸从菠菜中分离出来,然后利用钙离子将草酸从溶液中以沉淀(A)的形式分离,过滤后用酸重新溶解、蒸发、结晶(B).沉淀A的化学式是
(3)结晶B在热天平差热分析联用的仪器中加热,测得在0-120℃、120-450℃、450-800℃三区间失重率之比为9:14:22,确定B的化学式
(4)定量测定结晶中B的含量:取结晶固体0.1280g加入0.2mol/L 盐酸15mL(用量筒量取),使固体全部溶解,然后用0.0200mol/L 的KMnO4溶液滴定,至锥形瓶中紫色不褪,用去KMnO4溶液16.20mL.计算结晶中B百分含量
Ⅱ.25℃时,Ksp(CaSO4)=7.10×10-5.在1L0.1mol?L-1CaCl2溶液中加入1L0.2mol?L-1的Na2SO4溶液,充分反应后(假设混合后溶液的体积变化忽略不计)溶液中Ca2+物质的量的浓度为
查看习题详情和答案>>
(1)菠菜中铁的主要存在价态是
+2
+2
.(2)验证菠菜中草酸的存在要先把草酸从菠菜中分离出来,然后利用钙离子将草酸从溶液中以沉淀(A)的形式分离,过滤后用酸重新溶解、蒸发、结晶(B).沉淀A的化学式是
CaC2O4
CaC2O4
.(3)结晶B在热天平差热分析联用的仪器中加热,测得在0-120℃、120-450℃、450-800℃三区间失重率之比为9:14:22,确定B的化学式
CaC2O4?H2O
CaC2O4?H2O
,写出三个区间分解反应方程式CaC2O4?H2O═CaC2O4+H2O、CaC2O4═CaCO3+CO、CaCO3═CaO+CO2
CaC2O4?H2O═CaC2O4+H2O、CaC2O4═CaCO3+CO、CaCO3═CaO+CO2
.(4)定量测定结晶中B的含量:取结晶固体0.1280g加入0.2mol/L 盐酸15mL(用量筒量取),使固体全部溶解,然后用0.0200mol/L 的KMnO4溶液滴定,至锥形瓶中紫色不褪,用去KMnO4溶液16.20mL.计算结晶中B百分含量
92.4%
92.4%
.Ⅱ.25℃时,Ksp(CaSO4)=7.10×10-5.在1L0.1mol?L-1CaCl2溶液中加入1L0.2mol?L-1的Na2SO4溶液,充分反应后(假设混合后溶液的体积变化忽略不计)溶液中Ca2+物质的量的浓度为
1.42×10-3
1.42×10-3
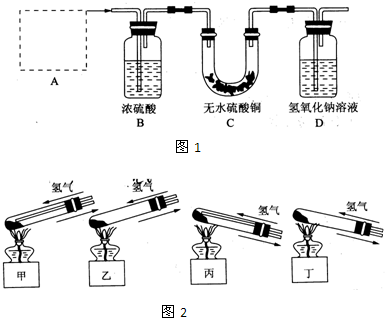
mol?L-1.Ⅰ、铜器长期暴露在潮湿空气中,它的表层往往含有“铜绿”(碱式碳酸铜),它受热易分解,为了从铜绿中制得铜,并测定铜绿在混合物中的质量分数,把铜绿样品放在试管中,与通入的纯净氢气在加热条件下发生反应,实验装置如图1,请回答下列有关问题.
(1)A处应选用图2装置中的(填写编号)
(2)反应开始前,对整个实验装置必须进行的操作是称量样品质量、检查装置的气密性和
(3)要测定铜绿在混合物中的质量分数,除需要知道样品质量外还需测定的实验数据是实验前后装置D质量.
(4)为使实验更准确,可采取的措施是
Ⅱ、10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为
(1)只要在加热煮沸后的溶液中加入足量的试剂X,若产生沉淀,则
A.Ba(OH)2溶液 B.BaC12溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
查看习题详情和答案>>
(1)A处应选用图2装置中的(填写编号)
丙
丙
(铁架台已省去),选用的理由是①因反应有水生成,试管口应略低于试管底部,防止冷凝水倒流到试管底部而使试管炸裂
因反应有水生成,试管口应略低于试管底部,防止冷凝水倒流到试管底部而使试管炸裂
;②通入氢气的导气管应伸入到试管底部,有利于将试管中的空气排净.
(2)反应开始前,对整个实验装置必须进行的操作是称量样品质量、检查装置的气密性和
称量装置D(含氢氧化钠溶液)的质量
称量装置D(含氢氧化钠溶液)的质量
;反应进行时,应先通氢气
通氢气
再加热
加热
;实验过程中,观察到试管中固体颜色变化为固体由绿色变黑色,最后变成光亮的红色
固体由绿色变黑色,最后变成光亮的红色
.(3)要测定铜绿在混合物中的质量分数,除需要知道样品质量外还需测定的实验数据是实验前后装置D质量.
(4)为使实验更准确,可采取的措施是
在D装置后加一个盛有碱石灰的球形干燥管
在D装置后加一个盛有碱石灰的球形干燥管
.Ⅱ、10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
.乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于
大于
(填“大小”或“小于”)NaHCO3.丙同学认为甲、乙的判断都不充分.丙认为:(1)只要在加热煮沸后的溶液中加入足量的试剂X,若产生沉淀,则
乙
乙
(填“甲”或“乙”)判断正确.试剂X是B
B
(填序号).A.Ba(OH)2溶液 B.BaC12溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则
甲
甲
(填“甲”或“乙”)判断正确.(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言
乙
乙
(填“甲”或“乙”)判断是错误的,理由是常压下加热NaHCO3的水溶液,溶液的温度达不到150℃
常压下加热NaHCO3的水溶液,溶液的温度达不到150℃
.