摘要:下列化合物中N的质量分数最高的是( ) A.NH4HCO3 B.NH4NO3 C.CO(NH2)2 D.NH4Cl
网址:http://m.1010jiajiao.com/timu3_id_328797[举报]
(2011?延庆县一模)A、B、C、D、E五种短周期元素,原子序数依次增大.A元素的单质是自然界最轻的气体,E单质须保存在煤油中.A与B、C分别构成电子数相等的化合物M、N,且M是一种能产生温室效应的最简单的有机气体物质;D元素最外层电子数是次外层电子数的3倍;
回答下列问题:
(1)N的电子式为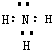
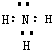 ;M分子中含有
;M分子中含有
(2)D与E以1:1形成的化合物与水反应的化学反应方程式
(3)A、B、C、D可形成阳离子和阴离子个数比是1:1的离子化合物X;A、D、E可形成化合物Y;X与Y以物质的量之比1:2加热反应,写出反应的化学方程式
(4)由N与D的单质、KOH溶液构成原电池,负极会产生C的单质.则其负极反应为
(5)在一定温度下,将4mol C单质和12mol A单质通入到体积为2L的密闭容器中,发生反应,2min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为
.从化学平衡移动的角度分析,提高A单质的转化率可以采取的措施是
a、及时分离出生成物 b、平衡后再加入6molA物质 c、增大压强 d、使用催化剂 e、平衡后再加入2molC物质.
查看习题详情和答案>>
回答下列问题:
(1)N的电子式为
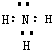
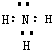
极性
极性
(填“极性”或“非极性”)键(2)D与E以1:1形成的化合物与水反应的化学反应方程式
2Na2O2+2CO2═2Na2CO3+O2↑
2Na2O2+2CO2═2Na2CO3+O2↑
(3)A、B、C、D可形成阳离子和阴离子个数比是1:1的离子化合物X;A、D、E可形成化合物Y;X与Y以物质的量之比1:2加热反应,写出反应的化学方程式
NH4HCO3+2NaOH
Na2CO3+NH3↑+2H2O
| ||
NH4HCO3+2NaOH
Na2CO3+NH3↑+2H2O
.反应后水溶液显
| ||
碱
碱
(填“酸”“碱”或“中”)性,原因是CO32-+H2O HCO3-+OH-
HCO3-+OH-
 HCO3-+OH-
HCO3-+OH-CO32-+H2O HCO3-+OH-
HCO3-+OH-
(用离子方程式表示) HCO3-+OH-
HCO3-+OH-(4)由N与D的单质、KOH溶液构成原电池,负极会产生C的单质.则其负极反应为
2NH3-6e-+6OH-═N2+6H2O
2NH3-6e-+6OH-═N2+6H2O
;一段时间后,溶液pH减小
减小
(填“增大”“减小”或“不变”).(5)在一定温度下,将4mol C单质和12mol A单质通入到体积为2L的密闭容器中,发生反应,2min达到平衡状态时,A单质的转化率是50%,则用A单质表示该反应的平均速率为
0.5mol/L-1min-1
0.5mol/L-1min-1
;该温度下的平衡常数为K=| 4 |
| 27 |
| 4 |
| 27 |
a、c、e
a、c、e
(选填序号字母).a、及时分离出生成物 b、平衡后再加入6molA物质 c、增大压强 d、使用催化剂 e、平衡后再加入2molC物质.