摘要:18.可燃性 溶解性
网址:http://m.1010jiajiao.com/timu3_id_32447[举报]
某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷着火点为40℃,红磷着火点为240℃,它们在空气中燃烧都会生成刺激呼吸道的白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按图A、图B所示装置进行对比实验: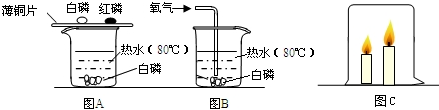
(1)用图A所示装置进行实验,观察到的现象是铜片上的白磷燃烧产生白烟:铜片上的红磷和水中的白磷不燃烧.再用图B所示装置进行实验,观察到:不通氧气时,热水中的白磷不燃烧;通氧气时,热水中的白磷燃烧.根据上述实验得出,可燃物燃烧的条件是
(2)根据燃烧的条件选择填空:用扇子扇炉火不会熄灭,而是越扇越旺,原因是
A.可快速地提供燃烧所需的氧气;
B.空气流动虽带走热量,但温度未降到着火点以下;
C.主要是空气流动带走热量,温度降到着火点以下.
(3)图A与图B所示实验相比,符合环保要求的是
(4)为探究实验后溶液的性质,在图B烧杯中滴入几滴石蕊试液,溶液呈红色,说明五氧化二磷与水反应所得溶液呈
【继续回答下列问题,你可以获得奖励分数,最多奖励4分,但化学总分不得超过60分】
(5)我们曾做过一个实验:向盛放有一高一低两支燃着的蜡烛的烧杯中倒入二氧化碳,发现的现象是下层的蜡烛比上层的蜡烛先熄灭.但如果将玻璃杯倒扣在两支燃着的蜡烛上(如上图C),蜡烛熄灭情况将如何?请提出你的猜想,并对你的猜想进行合理解释(提示:由于实验条件不同,使用玻璃杯的形状可能不同,如细长型、粗矮型等).
①
②
查看习题详情和答案>>

(1)用图A所示装置进行实验,观察到的现象是铜片上的白磷燃烧产生白烟:铜片上的红磷和水中的白磷不燃烧.再用图B所示装置进行实验,观察到:不通氧气时,热水中的白磷不燃烧;通氧气时,热水中的白磷燃烧.根据上述实验得出,可燃物燃烧的条件是
通常需要接触空气(或氧气),且温度达到着火点
通常需要接触空气(或氧气),且温度达到着火点
.(2)根据燃烧的条件选择填空:用扇子扇炉火不会熄灭,而是越扇越旺,原因是
AB
AB
;用扇子扇蜡烛的烛火一扇就立即熄灭,原因是C
C
(以上均填序号).A.可快速地提供燃烧所需的氧气;
B.空气流动虽带走热量,但温度未降到着火点以下;
C.主要是空气流动带走热量,温度降到着火点以下.
(3)图A与图B所示实验相比,符合环保要求的是
图B
图B
.(4)为探究实验后溶液的性质,在图B烧杯中滴入几滴石蕊试液,溶液呈红色,说明五氧化二磷与水反应所得溶液呈
酸性
酸性
.(填“酸性”、“碱性”)【继续回答下列问题,你可以获得奖励分数,最多奖励4分,但化学总分不得超过60分】
(5)我们曾做过一个实验:向盛放有一高一低两支燃着的蜡烛的烧杯中倒入二氧化碳,发现的现象是下层的蜡烛比上层的蜡烛先熄灭.但如果将玻璃杯倒扣在两支燃着的蜡烛上(如上图C),蜡烛熄灭情况将如何?请提出你的猜想,并对你的猜想进行合理解释(提示:由于实验条件不同,使用玻璃杯的形状可能不同,如细长型、粗矮型等).
①
上层蜡烛先熄灭,下层蜡烛后熄灭.解释:通常情况下,二氧化碳的密度比空气大,但由于热胀冷缩,蜡烛燃烧生成的热的二氧化碳气体体积变大,密度变得比空气的小,会聚集在玻璃杯的上方,使上方的蜡烛先熄灭
上层蜡烛先熄灭,下层蜡烛后熄灭.解释:通常情况下,二氧化碳的密度比空气大,但由于热胀冷缩,蜡烛燃烧生成的热的二氧化碳气体体积变大,密度变得比空气的小,会聚集在玻璃杯的上方,使上方的蜡烛先熄灭
.②
下层蜡烛先熄灭,上层蜡烛后熄灭.解释:二氧化碳的密度大于空气,蜡烛燃烧生成热的二氧化碳,在扩散过程中冷却后,会在玻璃杯中由下向上聚集,使下方的蜡烛先熄灭
下层蜡烛先熄灭,上层蜡烛后熄灭.解释:二氧化碳的密度大于空气,蜡烛燃烧生成热的二氧化碳,在扩散过程中冷却后,会在玻璃杯中由下向上聚集,使下方的蜡烛先熄灭
.化学研究性小组做酸碱中和实验.
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
| 盐溶液 | CaCl2溶液 | Na2CO3溶液 | NaCl溶液 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取少量样品于试管中, 加适量水振荡后全部溶解,滴 入CaCl2溶液至过量,充分反 应后,静置. | 白色沉淀 | 样品中一定含有______ |
| 步骤一:取步骤一充分反应后 的少量上层清液于试管中,滴 入无色酚酞试液至. | ______ | 结合两步实验得出 猜想一成立. |
[反思]NaOH固体应______保存. 查看习题详情和答案>>
化学研究性小组做酸碱中和实验.
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
[进行实验]请你与他们共同完成,并回答所给的问题:
[拓展]研究性小组同学在步骤二中滴加的试剂除用指示剂外,还可以用______替代.
[反思]NaOH固体应______保存.
查看习题详情和答案>>
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
| 盐溶液 | CaCl2溶液 | Na2CO3溶液 | NaCl溶液 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取少量样品于试管中, 加适量水振荡后全部溶解,滴 入CaCl2溶液至过量,充分反 应后,静置. |
白色沉淀 | 样品中一定含有______ |
| 步骤一:取步骤一充分反应后 的少量上层清液于试管中,滴 入无色酚酞试液至. |
______ | 结合两步实验得出 猜想一成立. |
[反思]NaOH固体应______保存.
化学研究性小组做酸碱中和实验.
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
[进行实验]请你与他们共同完成,并回答所给的问题:
[拓展]研究性小组同学在步骤二中滴加的试剂除用指示剂外,还可以用______替代.
[反思]NaOH固体应______保存.
查看习题详情和答案>>
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
| 盐溶液 | CaCl2溶液 | Na2CO3溶液 | NaCl溶液 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取少量样品于试管中, 加适量水振荡后全部溶解,滴 入CaCl2溶液至过量,充分反 应后,静置. | 白色沉淀 | 样品中一定含有______ |
| 步骤一:取步骤一充分反应后 的少量上层清液于试管中,滴 入无色酚酞试液至. | ______ | 结合两步实验得出 猜想一成立. |
[反思]NaOH固体应______保存.
查看习题详情和答案>>
化学研究性小组做酸碱中和实验.
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
[进行实验]请你与他们共同完成,并回答所给的问题:
[拓展]研究性小组同学在步骤二中滴加的试剂除用指示剂外,还可以用______替代.
[反思]NaOH固体应______保存.
查看习题详情和答案>>
Ⅰ.同学们在老师指导下,用氢氧化钠固体配制100g溶质质量分数为10%的氢氧化钠溶液.
(1)溶解时需要用到玻璃棒,其作用是______;
(2)下列操作会导致配制的氢氧化钠溶液溶质的质量分数偏低的是______(填序号)
A.氢氧化钠固体中含有不溶于水的杂质
B.用水洗净后的燃杯未干燥就直接用于配制
C.用量筒量取水的体积时采用俯视的方法读数
Ⅱ.当小组的同学将稀盐酸滴入所配制的氢氧化钠溶液进行中和实验时,发现有气泡产生,小组同学产生质疑,要对这瓶变质的氢氧化钠固体进行探究.
[分析]氢氧化钠固体曝露在空气中不仅吸收,还可以与空气中二氧化碳反应而变质,写出该反应的化学方程式______.
[猜想假设]猜想一:该氢氧化钠样品部分变质.
猜想二:该氢氧化钠样品全部变质.
[查阅资料]①已知反应:CaCl2+Na2CO3═2NaCl+CaCO3↓
②部分盐酸溶液的pH如下表:
| 盐溶液 | CaCl2溶液 | Na2CO3溶液 | NaCl溶液 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取少量样品于试管中, 加适量水振荡后全部溶解,滴 入CaCl2溶液至过量,充分反 应后,静置. | 白色沉淀 | 样品中一定含有______ |
| 步骤一:取步骤一充分反应后 的少量上层清液于试管中,滴 入无色酚酞试液至. | ______ | 结合两步实验得出 猜想一成立. |
[反思]NaOH固体应______保存.
查看习题详情和答案>>