摘要:23.⑴ C6H6 +Br2 → C6H5Br + HBr ⑵ 反应液微沸 有红棕色气体充满A容器 ⑶ 除去溶于溴苯中的溴 ⑷ 除去溴化氢气体中的溴蒸气 ⑸ 石蕊试液.溶液变红色
网址:http://m.1010jiajiao.com/timu3_id_322465[举报]
 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.(1)写出A中反应的化学方程式
C6H6+Br2
C6H5Br+HBr
| Fe |
C6H6+Br2
C6H5Br+HBr
| Fe |
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
除去溶于溴苯中的溴
除去溶于溴苯中的溴
,写出有关反应的离子方程式Br2+2OH-═Br-+BrO-+H2O
Br2+2OH-═Br-+BrO-+H2O
.(3)C中盛放CCl4的作用是
除去溴化氢气体中的溴蒸气
除去溴化氢气体中的溴蒸气
.(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明.另一种验证的方法是向试管D中加入
石蕊试液
石蕊试液
,现象是溶液变红色
溶液变红色
. 人们对苯的结构及性质的认识经历了一个漫长的过程.
人们对苯的结构及性质的认识经历了一个漫长的过程.(1)实验测得苯的分子式为C6H6,与烷烃相比,6个碳原子应结合14个氢原子才能达到饱和,写出C6H6的一种含叁键且无支链链烃(注意:C周围四对共用电子对除碳碳叁键外其他碳原子达到饱和)的结构简式
CH≡C-C≡C-CH2-CH3
CH≡C-C≡C-CH2-CH3
.(2)既然苯中含有双键或三键等不饱和键,苯应该能使溴水褪色,但实验发现,将溴水滴入苯中,只是出现了分层现象.若将溴水换成液溴,加入少量铁粉,可发生剧烈反应.
某化学课外小组用图装置使苯与液溴反应.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
①实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
除去溶于溴苯中的溴
除去溶于溴苯中的溴
反应的方程式Br2+2NaOH→NaBr+NaBrO+H2O
Br2+2NaOH→NaBr+NaBrO+H2O
②A中反应的化学方程式
 +Br
+Br| 催化剂 |
 -Br+HBr
-Br+HBr +Br
+Br| 催化剂 |
 -Br+HBr
-Br+HBr反应类型:
取代反应
取代反应
③能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明.另一种验证的方法是向试管D中加入
石蕊试液
石蕊试液
,现象是溶液变红色
溶液变红色
.(3)1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决.它不能解释下列哪些事实
AD
AD
A.苯不能使酸性高锰酸钾溶液褪色 B.溴苯没有同分异构体
C.1mol苯能与3molH2加成 D.邻二溴苯只有一种
(4)现代化学认为苯分子碳碳之间的键是
介于单键和双键之间的特殊的键
介于单键和双键之间的特殊的键
.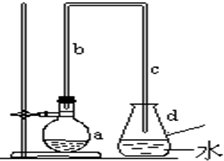 实验室用如图装置制取少量溴苯.
实验室用如图装置制取少量溴苯.(1)在烧瓶a中装的试剂是
苯
苯
、液溴
液溴
和铁
铁
.导管b的作用有两个:一是导气
导气
,二是兼起冷凝
冷凝
的作用.(2)反应过程中在导管c的下口附近可以观察到有
白雾
白雾
出现,这是由于反应生成的HBr
HBr
遇水蒸气而形成的.(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液有
浅黄色沉淀生成
浅黄色沉淀生成
生成,写出离子方程式:Ag++Br-=AgBr↓
Ag++Br-=AgBr↓
.(4)反应完毕后,将烧瓶中a的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有
褐
褐
色不溶于水的液体.这是因为溴苯中溶解了溴单质
溶解了溴单质
.纯溴苯是无
无
色液
液
体,除去杂质所需的试剂是氢氧化钠溶液
氢氧化钠溶液
,用分液
分液
方法分离.(5)写出烧瓶a中发生反应的化学方程式:
C6H6+Br2
C6H5Br+HBr
| Fe |
C6H6+Br2
C6H5Br+HBr
.| Fe |