摘要:23. (1)Na+[:O:O:]2-Na+ 离子键.非极性共价键 (2)H++HSO3-=H2O+SO2↑
网址:http://m.1010jiajiao.com/timu3_id_322130[举报]
填写空格
(1)写出下列物质的电子式:N2
 ;HClO
;HClO
 ;
;
(2)写出下列物质的结构式:CH4
 ; CO2
; CO2
(3)与Ar原子电子层结构相同的-2价阴离子的离子结构示意图
 .
.
(4)在1-18号元素组成的化合物中具有三核10个电子的共价化合物是
(5)下列叙述中所涉及元素是氧元素的有
a.质量数为18,原子核中有10个中子的核素
b.核电荷数等于最外层电子数的离子
c.质子数等于短周期同族元素原子序数一半的元素
d.原子的最外层电子数是内层电子数3倍的元素
e.能与H、C、N、Na、S、Fe等元素形成两种或两种以上的化合物的元素
f.形成化合物的种类最多的元素
g.Y和Z均由元素R组成,反应Y+2I-+2H+ I2+Z+H2O,其中的R元素.
I2+Z+H2O,其中的R元素.
查看习题详情和答案>>
(1)写出下列物质的电子式:N2




(2)写出下列物质的结构式:CH4


O═C═O
O═C═O
.(3)与Ar原子电子层结构相同的-2价阴离子的离子结构示意图


(4)在1-18号元素组成的化合物中具有三核10个电子的共价化合物是
H2O
H2O
;具有三核20个电子的离子化合物是LiHS或NaOH
LiHS或NaOH
;具有四核18个电子的两种化合物分别是H2O2
H2O2
、PH3
PH3
;既具有离子键又有非极性键和极性键的化合物是CH3COONa
CH3COONa
.(5)下列叙述中所涉及元素是氧元素的有
abcdeg
abcdeg
a.质量数为18,原子核中有10个中子的核素
b.核电荷数等于最外层电子数的离子
c.质子数等于短周期同族元素原子序数一半的元素
d.原子的最外层电子数是内层电子数3倍的元素
e.能与H、C、N、Na、S、Fe等元素形成两种或两种以上的化合物的元素
f.形成化合物的种类最多的元素
g.Y和Z均由元素R组成,反应Y+2I-+2H+
 I2+Z+H2O,其中的R元素.
I2+Z+H2O,其中的R元素.(2012?大兴区一模)下表为元素周期表的一部分,请参照①-⑨相关元素在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)由②④⑤三种元素组成的物质的水溶液显碱性,用离子方程式表示溶液显碱性的原因:
(4)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,则该化合物的电子式为:
 ,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:
,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:
(5)以⑥的单质材料为阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成有吸附性的难溶物R,写出阳极生成R的电极反应式:
(6)化学方程式:A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应类型,A、B、X、Y是中学常见的物质,下列反应中A都为单质,请回答:
(ⅰ)若A为红色固体,在加热条件下反应产生有刺激性气味、有漂白作用的气体,写出检验该气体的方法
(ⅱ)若A为黑色粉末,少量A和B常温下反应生成的Y是无色气体,且Y无色,该气体在空气中易变成红棕色,写出常温下少量A和B反应的化学方程式:
(iii)若B为白色乳状物,且溶解度随温度的升高而降低,Y可做固体干燥剂,则该反应在工业上可用于制备
查看习题详情和答案>>
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | |||||
Na>Al>O
Na>Al>O
.(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
HNO3>H2CO3>H2SiO3
HNO3>H2CO3>H2SiO3
.(3)由②④⑤三种元素组成的物质的水溶液显碱性,用离子方程式表示溶液显碱性的原因:
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
(4)甲、乙是由②③④三种元素中一种或两种元素形成的双原子分子或负二价阴离子,它们的电子总数相等,甲与钙元素组成的化合物既含离子键又含非极性共价键,则该化合物的电子式为:


3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
| ||
(5)以⑥的单质材料为阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成有吸附性的难溶物R,写出阳极生成R的电极反应式:
Al-3e-=Al3+,Al3++3HCO3-═Al(OH)3↓+3CO2↑或Al-3e-+3HCO3-═Al(OH)3↓+3CO2↑
Al-3e-=Al3+,Al3++3HCO3-═Al(OH)3↓+3CO2↑或Al-3e-+3HCO3-═Al(OH)3↓+3CO2↑
(6)化学方程式:A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应类型,A、B、X、Y是中学常见的物质,下列反应中A都为单质,请回答:
(ⅰ)若A为红色固体,在加热条件下反应产生有刺激性气味、有漂白作用的气体,写出检验该气体的方法
将气体X通入品红溶液中,若品红溶液褪色,加热恢复红色,证明气体X是SO2
将气体X通入品红溶液中,若品红溶液褪色,加热恢复红色,证明气体X是SO2
(ⅱ)若A为黑色粉末,少量A和B常温下反应生成的Y是无色气体,且Y无色,该气体在空气中易变成红棕色,写出常温下少量A和B反应的化学方程式:
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
(iii)若B为白色乳状物,且溶解度随温度的升高而降低,Y可做固体干燥剂,则该反应在工业上可用于制备
漂白粉
漂白粉
.(1)
纳米材料二氧化钛(TiO2)可做优良的催化剂.据报道:“生态马路”是在铺设时加入一定量的
TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:a
.O2→2Ob
.O+H2O→2OHc
.OH+OH→H2O2①B中破坏的是________(填“极性共价键”或“非极性共价键”).
②H2O2
能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的作用是________(填“氧化性”或“还原性”).(2)某固体混合物中含有Na+、K+、Mg2+和Cl-、Br-五种微粒.
Ⅰ.欲将钠、钾、镁三元素大致分离开来,并将氯、溴两元素大致分离开来,有以下方法和操作步骤可供选择(其中有的步骤可选两次).
①溶于水制成稀溶液;
②溶于水制成浓溶液;
③通入足量CO2;
④加入足量氯水;
⑤通入足量氨气;
⑥过滤;
⑦用四氯化碳萃取.
选取最合理的方法和步骤:(按顺序先后填写编号)________.
Ⅱ.分离后剩余的水溶液中所含的主要物质是________.
Ⅲ.在上述分离过程中分离出一种化合物晶体.欲得到干燥的该化合物固体,有两种方法可供选择:①加热蒸发掉水分;②将过滤得到的固体物质自然风干.正确的方法应选择________.
根据下列某些短周期元素中元素性质的有关信息,回答下列问题:
(1)元素①②⑧的第一电离能由大到小的顺序是
(2)元素⑤⑥⑦中的某两种形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有
(3)某元素R 的原子半径为1.02×10-10m,它与钠形成Na2R2,若物质Na2R2是一种含有非极性共价键的离子化合物,其电子式是
 (R用元素符号表示).
(R用元素符号表示).
(4)元素①和⑨形成阳离子,其结构式为
 ,其中心原子以
,其中心原子以
(5)元素⑤的原子基态电子排布式为
查看习题详情和答案>>
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径 /10-10m |
0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52] | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |
H、Li、Na
H、Li、Na
;元素③⑥⑨的电负性由大到小的顺序是O、N、P
O、N、P
(以上均用元素符号填空).(2)元素⑤⑥⑦中的某两种形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有
CCl4、PCl3
CCl4、PCl3
(写化学式).(3)某元素R 的原子半径为1.02×10-10m,它与钠形成Na2R2,若物质Na2R2是一种含有非极性共价键的离子化合物,其电子式是


(4)元素①和⑨形成阳离子,其结构式为


sp3
sp3
杂化轨道成键.(5)元素⑤的原子基态电子排布式为
1s22s22p2
1s22s22p2
.【化学——选修3:物质结构与性质】(15分)
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6] (NO3)3 [三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。 Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型);
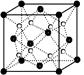
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如右图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长 a = cm。 (用含ρ、NA的计算式表示)
(3)下列有关的说法正确的是 。
E.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。回答下列问题:
① Y2X2分子中Y原子轨道的杂化类型为 ,1mol Y2X2含有σ键的数目为
。
② 化合物ZX3的沸点比化合物YX4的高,其主要原因是 。
③ 元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 。
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6] (NO3)3 [三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。
①基态Fe3+的M层电子排布式为 。
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x= 。 Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型);
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如右图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长 a = cm。 (用含ρ、NA的计算式表示)

(3)下列有关的说法正确的是 。
| A.第一电离能大小:S>P>Si |
| B.电负性顺序:C<N<O<F |
| C.因为晶格能CaO比KCl高,所以KCl比CaO熔点低 |
| D.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大 |
(4)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。回答下列问题:
① Y2X2分子中Y原子轨道的杂化类型为 ,1mol Y2X2含有σ键的数目为
。
② 化合物ZX3的沸点比化合物YX4的高,其主要原因是 。
③ 元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 。