摘要:下列叙述不正确的是 ( ) A.化学平衡发生移动.平衡常数不一定发生变化 B.升高温度会增大化学反应速率.其原因是增加 了活化分子的百分数 C.某化学反应的能量变化如右图所示.则该反应的 △H>0.△S>0 D.H3PO4的电离常数:K1>>K2>>K3
网址:http://m.1010jiajiao.com/timu3_id_321985[举报]
下列叙述不正确的是
A.化学平衡发生移动,平衡常数不一定发生变化
B.升高温度会增大化学反应速率,其原困是增加了活化分子的百分数
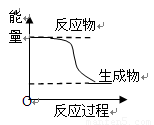
C.某化学反应的能量变化如上图所示,则该反应的△H>0.△S>0
D.H3PO4的电离常数:Kal>>Ka2>>Ka3
查看习题详情和答案>>
下列叙述不正确的是

A.化学平衡发生移动,平衡常数不一定发生变化
B.升高温度会增大化学反应速率,其原因是增加了活化分子的百分数
C.某化学反应的能量变化如上图所示,则该反应的△H>0,△S>0
D.H3PO4的电离常数:K1>>K2>>K3
查看习题详情和答案>>
下列叙述不正确的是( )
| A.化学平衡发生移动,平衡常数不一定发生变化 |
| B.升高温度会增大化学反应速率,其原因是增大了活化分子的百分数 |
C.某化学反应的能量变化如图所示,则该反应的ΔH>0,ΔS>0 |
D.H3PO4的电离常数:  |
