摘要:将CoCl2溶解于盐酸中可形成CoCl42-.在溶液中存在着下面化学平衡:Co2++4Cl-CoCl42-△H>0下列说法正确的是( ) A.升高温度.正反应速率增大.逆反应速率减小 B.该反应的平衡常数K=C(CoCl42-)/C(Co2+)×C4(Cl-) C.将盛有CoCl2和盐酸混合溶液的试管置于热水中.试管内溶液为红色 D.增大Cl-浓度.平衡向正反应方向移动.Co2+.Cl-浓度都减小 17.根据下列操作.选出对溶液的酸碱性无影响的正确组合( ) ①向氯化钠溶液中滴加硫酸氢钠溶液 ②向醋酸溶液中加入醋酸钠固体 ③加热0.1mol/L的盐酸溶液至沸腾 ④加热蔗糖溶液使其温度从25℃升至50℃ ⑤向稀氨水加入NaCl固体 ⑥向20mL0.1mol/LBa(OH)2溶液中加入60ml0.2mol/LNaOH溶液 A.③④ B.④⑤⑥ C.②③⑤ D.①③④⑤⑥
网址:http://m.1010jiajiao.com/timu3_id_315066[举报]
将CoCl2溶解于盐酸中可以形成CoCl42-,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq)?CoCl
(aq)△H>0
粉红色 蓝色
下列说法正确的是( )
Co2+(aq)+4Cl-(aq)?CoCl
2- 4 |
粉红色 蓝色
下列说法正确的是( )
将CoCl2溶解于盐酸中可以形成CoCl,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq)  CoCl(aq) ΔH>0
CoCl(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
A.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
B.升高温度,正反应速率增大,逆反应速率减小
C.该反应的平衡常数K=
D.增大Cl-浓度,平衡向正反应方向移动,试管内溶液变为蓝色
查看习题详情和答案>>
将CoCl2溶解于盐酸中可以形成CoCl42—,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl42—(aq) ΔH>0
CoCl42—(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
A.升高温度,正反应速率增大,逆反应速率减小
B.该反应的平衡常数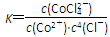
C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小
查看习题详情和答案>>
将CoCl2溶解于盐酸中可以形成CoCl42—,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl42—(aq) ΔH>0
CoCl42—(aq) ΔH>0
粉红色 蓝色
下列说法正确的是( )
| A.升高温度,正反应速率增大,逆反应速率减小 |
B.该反应的平衡常数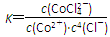 |
| C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色 |
| D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小 |