网址:http://m.1010jiajiao.com/timu3_id_308403[举报]
__________。
(2)B与C比较,电负性较小的是_______(填元素符号);B与C形成的化合物晶体类型是_________。
(3)E属元素周期表中第_____周期,第______族的元素,其元素名称是________,它的+2价离子的电子排布式为__________。
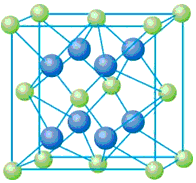
(4)从图中可以看出,D跟B形成的离子化合物的化学式为__________;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是__________(只要求列出算式)。
已知A、B、c、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D和E属同一周期,又知E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,D跟B可形成离子化合物,其晶胞结构如右图。请回答:
(1)A与c形成的共价化合物的分子式是 ,杂化轨道是____,分子的立体结构是____。
(2)B与C比较,电负性较小的是 (填元素符号);B与c形成的化合物晶体类型是 。
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 ,
它的+2价离子的电子排布式为 。
(4)从图中可以看出,D踉B形成的离子化合物的化学式为 ;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是 (只要求列出算式)。
查看习题详情和答案>>(14分)
现有A、B、C、D、E、F六种短周期元素,A、E处于同一主族且E是短周期元素中原子半径最大的元素(不含稀有气体)。已知C的原子序数等于A、B的原子序数之和,D的原子序数等于A、C的原子序数之和。人类已知的化合物中,有一类化合物的种类已超过三千万,这类化合物中一般都含有A、B两种元素。F是一种生活中常用的金属。根据以上信息,回答下列问题:
(1)元素B在周期表中的位置是 。
(2)F的单质与E的最高价氧化物对应水化物反应的化学方程式是 。
(3)C、D最低价氢化物稳定性的强弱顺序是 (填化学式) ;D、E、F原子半径的大小顺序是 (填元素符号)。
(4)在A、C、D组成的化合物中,既有离子键又有共价键的是 (填化学式)。
(5)在A、B、D中,由两种或三种元素组成两种可以反应的阴离子,该反应的离子方程式是 。
(6)化合物BA4D与O2、稀硫酸可组成燃料电池,此电池的负极反应式是 。
查看习题详情和答案>>
(14分)
现有A、B、C、D、E、F六种短周期元素,A、E处于同一主族且E是短周期元素中原子半径最大的元素(不含稀有气体)。已知C的原子序数等于A、B的原子序数之和,D的原子序数等于A、C的原子序数之和。人类已知的化合物中,有一类化合物的种类已超过三千万,这类化合物中一般都含有A、B两种元素。F是一种生活中常用的金属。根据以上信息,回答下列问题:
(1)元素B在周期表中的位置是 。
(2)F的 单质与E的最高价氧化物对应水化物反应的化学方程式是 。
单质与E的最高价氧化物对应水化物反应的化学方程式是 。
(3)C、D最低价氢化物稳定性的强弱顺序是 (填化学式) ;D、E、F原子半径的大小顺序是 (填元素符号)。
(4)在A、C、D组成的化合物中,既有离子键又有共价键的是 (填化学式)。
(5)在A、B、D中,由两种或三种元素组成两种可以反应的阴离子,该反应的离子方程式是 。
(6)化合物BA4D与O2、稀硫酸可组成燃 料电池,此电池的负极反应式是 。
料电池,此电池的负极反应式是 。
(14分)
现有A、B、C、D、E、F六种短周期元素,A、E处于同一主族且E是短周期元素中原子半径最大的元素(不含稀有气体)。已知C的原子序数等于A、B的原子序数之和,D的原子序数等于A、C的原子序数之和。人类已知的化合物中,有一类化合物的种类已超过三千万,这类化合物中一般都含有A、B两种元素。F是一种生活中常用的金属。根据以上信息,回答下列问题:
(1)元素B在周期表中的位置是 。
(2)F的单质与E的最高价氧化物对应水化物反应的化学方程式是 。
(3)C、D最低价氢化物稳定性的强弱顺序是 (填化学式) ;D、E、F原子半径的大小顺序是 (填元素符号)。
(4)在A、C、D组成的化合物中,既有离子键又有共价键的是 (填化学式)。
(5)在A、B、D中,由两种或三种元素组成两种可以反应的阴离子,该反应的离子方程式是 。
(6)化合物BA4D与O2、稀硫酸可组成燃料电池,此电池的负极反应式是 。
查看习题详情和答案>>