摘要:硫在空气中燃烧 点燃 ==== S + O2 SO2 现象:在空气中是发出微弱的淡蓝色火焰.在氧气中是发出明亮的蓝紫色火焰. 相关知识点:反应后的产物可用紫色的石蕊来检验
网址:http://m.1010jiajiao.com/timu3_id_3063[举报]
淡黄色
淡黄色
色的硫粉在空气中燃烧火焰呈淡蓝色
淡蓝色
色.而在氧气中燃烧,发出蓝紫色
蓝紫色
色火焰,且生成无色刺激性
刺激性
气味的气体.该反应的文字表达式为:硫+氧气
二氧化硫
| 点燃 |
硫+氧气
二氧化硫
;用符号表示为:| 点燃 |
S+O2
SO2
| ||
S+O2
SO2
.做铁丝在氧气中燃烧的实验时,为了防止溅落的熔化物炸裂瓶底,集气瓶里预先要装
| ||
少量的水或铺一层细沙
少量的水或铺一层细沙
,该反应的文字表达式为:铁+氧气
四氧化三铁
| 点燃 |
铁+氧气
四氧化三铁
.符号表达式为:| 点燃 |
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
.
| ||
图A、B、C是兵兵完成物质在氧气中的燃烧实验示意图,我们一起来探讨相关问题.
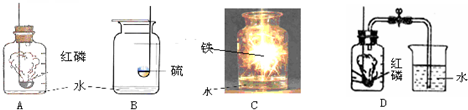
(1)在图A试验中,我们可以观察到的实验现象是
【反思拓展】
如果用燃烧法来测定空气中氧气的体积分数,不能选用镁条,因为镁条除了和氧气反应,还要和氮气等反应;也不能选用铁丝,其原因是
(2)在图B的实验中,肉眼可以看到
(3)兵兵认为图C实验的现象为:
查看习题详情和答案>>

(1)在图A试验中,我们可以观察到的实验现象是
红磷燃烧,发出黄色火焰,产生大量白烟,放出热量
红磷燃烧,发出黄色火焰,产生大量白烟,放出热量
;该反应的符号表达式为4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.教材中我们也用该反应进行空气中氧气含量的测定,如图D,在该实验中,如果实验时红磷的量不足,可能导致结果
| ||
偏小
偏小
.【反思拓展】
如果用燃烧法来测定空气中氧气的体积分数,不能选用镁条,因为镁条除了和氧气反应,还要和氮气等反应;也不能选用铁丝,其原因是
铁丝在空气中不能燃烧
铁丝在空气中不能燃烧
;一般也不会选用木炭或硫粉,其原因是产生的气体占据了消耗掉的氧气的空间,压强不变
产生的气体占据了消耗掉的氧气的空间,压强不变
.请结合所学知识,总结“用燃烧法测定空气中氧气的体积分数”时,对选用的反应物生成物分别有何要求:反应物在空气中能燃烧
反应物在空气中能燃烧
,生成物不能产生气体
生成物不能产生气体
.但将D中集气瓶中的水改为另一种液体氢氧化钙溶液
氢氧化钙溶液
,重复上述实验,发现液体浑浊,有倒吸现象.(2)在图B的实验中,肉眼可以看到
明亮蓝紫色火焰
明亮蓝紫色火焰
,实验时,燃烧匙伸入集气瓶的正确做法是从上至下缓慢伸入
从上至下缓慢伸入
,该实验中集气瓶底的水所起作用是吸收SO2,避免污染空气
吸收SO2,避免污染空气
.该反应的符号表达式为S+O2
SO2
| ||
S+O2
SO2
.
| ||
(3)兵兵认为图C实验的现象为:
剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体
剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体
.写出下列反应的文字或符号表达式,并注明反应的基本类型:
(1)硫在空气中燃烧:
(2)氯酸钾和二氧化锰混合物加热:
(3)任写一个既是化合反应又是氧化反应的例子:
查看习题详情和答案>>
(1)硫在空气中燃烧:
硫+氧
二氧化硫或S+O2
SO2(化合反应)
| 点燃 |
| ||
硫+氧
二氧化硫或S+O2
SO2(化合反应)
;| 点燃 |
| ||
(2)氯酸钾和二氧化锰混合物加热:
氯酸钾
氯化钾+氧气或2KClO3
2KCl+3O2 ↑(分解反应)
| 二氧化锰 |
| 加热 |
| ||
| △ |
氯酸钾
氯化钾+氧气或2KClO3
2KCl+3O2 ↑(分解反应)
;| 二氧化锰 |
| 加热 |
| ||
| △ |
(3)任写一个既是化合反应又是氧化反应的例子:
碳+氧气
二氧化碳或C+O2
CO2
| 点燃 |
| ||
碳+氧气
二氧化碳或C+O2
CO2
.| 点燃 |
| ||
酸雨是pH小于5.6的降水.我国大部分地区所降酸雨主要是由居民和工厂燃烧含硫的煤以及某些化工厂生产过程中排放的二氧化硫气体,经过一系列化学反应而形成的.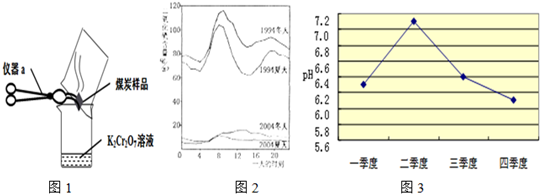
(1)如果硫粉在氧气中燃烧,观察到的现象是
(2)几位同学为了探究木炭中是否含有少量硫元素,他们设计了如图1所示实验进行测定.请写出图中仪器a的名称: +H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
+H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
(3)如图2是1994年和2004年某城市的一天各个时刻测到的空气中二氧化硫的含量.下列说法不正确的是
A.曲线显示冬天大气中的二氧化硫含量比夏天高
B.曲线显示了1994年一天中大约8点左右二氧化硫的含量较高
C.二氧化硫的含量在10年间降低的原因可能是加强了燃料的脱硫和控制了二氧化硫的排放
D.二氧化硫污染的主要来源是汽车排放的尾气,控制污染的方法是禁止使用汽车
(4)在研究酸雨危害的过程中,测定该地区雨水的pH的实验操作
某化学兴趣小组取刚降到地面的雨水,每隔一定时间用较精密的pH计测定其pH,数据如下:
由此可知该雨水的酸性越来越
(5)酸雨造成的危害很多.某兴趣小组调查发现某市的石刻的表面有不同程度的腐蚀.且近20年的腐蚀速度大大超过以往,其中最主要原因之一就是酸雨.为了减缓石刻腐蚀,请你提一条建议:
酸雨还会使土壤酸化.为了中和酸性土壤,可以使用熟石灰粉末,若该酸雨的成分是硫酸,请写出该中和反应的化学方程式
(6)某校化学兴趣小组在学完碱的化学性质后,想到用NaOH溶液吸收SO2,反应化学方程式如下:2NaOH+SO2═Na2SO3+H2O 用NaOH溶液吸收1000L已除去CO2的空气样品,溶液质量增重了0.64g.已知此时空气的密度约为1.3g/L,求:
①被吸收的SO2的质量
②发生反应的NaOH的质量.(相对原子质量:Na-23 S-32 O-16)
③空气中SO2的质量分数(计算结果精确到0.01%).
查看习题详情和答案>>

(1)如果硫粉在氧气中燃烧,观察到的现象是
剧烈燃烧,放出热量,产生明亮的蓝紫色火焰,产生一种无色有刺激性气味的气体
剧烈燃烧,放出热量,产生明亮的蓝紫色火焰,产生一种无色有刺激性气味的气体
,该反应的化学方程式为S+O2
SO2
| ||
S+O2
SO2
.
| ||
(2)几位同学为了探究木炭中是否含有少量硫元素,他们设计了如图1所示实验进行测定.请写出图中仪器a的名称:
坩埚钳
坩埚钳
.他们查阅资料后得知:“二氧化硫能使K2Cr2O7溶液褪色(由橙红色变成绿色),反应方程式为:“3SO2+K2Cr2O7+H2SO4═K2SO4+ +H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:
+H2O”.然而化学方程式中有一生成物不清楚,请根据已学知识推测其化学式:Cr2(SO4)3
Cr2(SO4)3
.反应前K2Cr2O7中Cr元素化合价为+6
+6
价.(3)如图2是1994年和2004年某城市的一天各个时刻测到的空气中二氧化硫的含量.下列说法不正确的是
D
D
A.曲线显示冬天大气中的二氧化硫含量比夏天高
B.曲线显示了1994年一天中大约8点左右二氧化硫的含量较高
C.二氧化硫的含量在10年间降低的原因可能是加强了燃料的脱硫和控制了二氧化硫的排放
D.二氧化硫污染的主要来源是汽车排放的尾气,控制污染的方法是禁止使用汽车
(4)在研究酸雨危害的过程中,测定该地区雨水的pH的实验操作
用玻璃棒蘸取雨水,点在试纸上,与标准比色卡对照,读取数值
用玻璃棒蘸取雨水,点在试纸上,与标准比色卡对照,读取数值
.某化学兴趣小组取刚降到地面的雨水,每隔一定时间用较精密的pH计测定其pH,数据如下:
| 测定时间/分钟 | 0 | 1 | 2 | 3 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
强
强
(填“强”或“弱”),最终趋于稳定.可能的原因是雨水中的H2SO3被氧气氧化为H2SO4,化学方程式为2H2SO3+O2=2H2SO4
2H2SO3+O2=2H2SO4
.(5)酸雨造成的危害很多.某兴趣小组调查发现某市的石刻的表面有不同程度的腐蚀.且近20年的腐蚀速度大大超过以往,其中最主要原因之一就是酸雨.为了减缓石刻腐蚀,请你提一条建议:
使用清洁能源
使用清洁能源
.酸雨会使河流、湖泊酸化.如图3是某市去年某河流一年中不同时期河水的平均pH变化的折线图.则去年河水酸性最强的季度是第四
四
季度.该季度雨水酸性最强的原因可能是:(答两条)冬季取暖,需要燃烧大量化石燃料,加大了对河水的污染
冬季取暖,需要燃烧大量化石燃料,加大了对河水的污染
;冬季降水量减少,河水中酸的浓度增大
冬季降水量减少,河水中酸的浓度增大
.酸雨还会使土壤酸化.为了中和酸性土壤,可以使用熟石灰粉末,若该酸雨的成分是硫酸,请写出该中和反应的化学方程式
H2SO4+Ca(OH)2=CaSO4+2H2O
H2SO4+Ca(OH)2=CaSO4+2H2O
.(6)某校化学兴趣小组在学完碱的化学性质后,想到用NaOH溶液吸收SO2,反应化学方程式如下:2NaOH+SO2═Na2SO3+H2O 用NaOH溶液吸收1000L已除去CO2的空气样品,溶液质量增重了0.64g.已知此时空气的密度约为1.3g/L,求:
①被吸收的SO2的质量
0.8
0.8
g.②发生反应的NaOH的质量.(相对原子质量:Na-23 S-32 O-16)
③空气中SO2的质量分数(计算结果精确到0.01%).
用化学反应符号表达式表示下列反应,并填空,反应类型指基本反应类型.
(1)硫在氧气中燃烧
(2)水通电分解
(3)铁丝在氧气中燃烧
(4)氢气在氯气中燃烧生成氯化氢
(5)实验室用氯酸钾和二氧化锰的混合物制取氧气
查看习题详情和答案>>
(1)硫在氧气中燃烧
S+O2
SO2
| ||
S+O2
SO2
,实验时常在集气瓶中放少量
| ||
水
水
以吸收生成的有害气体.(2)水通电分解
2H2O
2H2↑+O2 ↑
| ||
2H2O
2H2↑+O2 ↑
,为检验正极产生的气体可用的方法是
| ||
用带火星(燃着)的木条检验
用带火星(燃着)的木条检验
,若正极产生气体的体积为x mL,则负极产生气体的体积为2x
2x
mL.(3)铁丝在氧气中燃烧
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
,实验前要将铁丝打磨光亮,目的是
| ||
除去表面的铁锈和油污,否则会影响实验进行
除去表面的铁锈和油污,否则会影响实验进行
.(4)氢气在氯气中燃烧生成氯化氢
H2+Cl2
2HCl
| ||
H2+Cl2
2HCl
,该反应属
| ||
化合
化合
反应.(5)实验室用氯酸钾和二氧化锰的混合物制取氧气
2KClO3
2KCl+3O2 ↑
| ||
| △ |
2KClO3
2KCl+3O2 ↑
,该反应属
| ||
| △ |
分解
分解
反应.该反应中,二氧化锰在固体混合物中的质量或质量分数符合下列图示的是AD
AD
(填字母序号).