网址:http://m.1010jiajiao.com/timu3_id_304818[举报]
已知A为固态物质,实验室利用A与水反应制备气态物质B;F遇到FeCl3溶液显紫色;I 属于二元醇.各物质间的转化关系如下图所示:
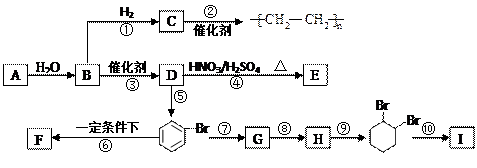 |
(1)请写出A的电子式____________________;反应⑤中加入的试剂是 .
写出结构简式: E ; F ;G ;H .
(2)以上各步反应中属于加成反应的有: ;属于取代反应的有: ;属于消去反应的有: ;属于聚合反应的有: 。(用序号填空)
(3)写出下列化学反应方程式
反应②________________________________________________________
反应④_______________________________________________________
反应⑧_______________________________________________________
反应⑩________________________________________________________
(4)写出1mol 物质I与足量的醋酸在浓硫酸加热条件下充分反应生成二元酯的方程式:
_________________________________________________________
写出F与Na2CO3溶液反应的离子方程式:
____________________________________________________________________________
(5)已知物质B在一定条件下可以转变成甲醛,请写出甲醛与银氨溶液反应的离子方程式:
__________________________________________________________ 查看习题详情和答案>>
已知A为固态物质,实验室利用A与水反应制备气态物质B;F遇到FeCl3溶液显紫色;I 属于二元醇.各物质间的转化关系如下图所示:
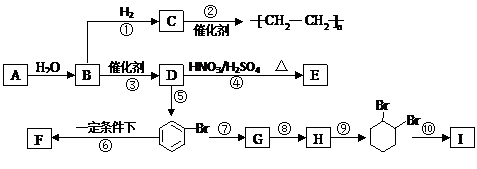 |
(1)请写出A的电子式____________________;反应⑤中加入的试剂是 .
写出结构简式: E ; F ;G ;H .
(2)以上各步反应中属于加成反应的有: ;属于取代反应的有: ;属于消去反应的有: ;属于聚合反应的有: 。(用序号填空)
(3)写出下列化学反应方程式
反应②________________________________________________________
反应④_______________________________________________________
反应⑧_______________________________________________________
反应⑩________________________________________________________
(4)写出1mol 物质I与足量的醋酸在浓硫酸加热条件下充分反应生成二元酯的方程式:
_________________________________________________________
写出F与Na2CO3溶液反应的离子方程式:
____________________________________________________________________________
(5)已知物质B在一定条件下可以转变成甲醛,请写出甲醛与银氨溶液反应的离子方程式:
__________________________________________________________
查看习题详情和答案>>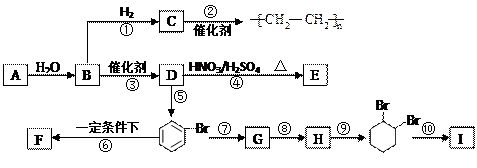 |
(1)请写出A的电子式____________________;反应⑤中加入的试剂是 .
写出结构简式: E ; F ;G ;H .
(2)以上各步反应中属于加成反应的有: ;属于取代反应的有: ;属于消去反应的有: ;属于聚合反应的有: 。(用序号填空)
(3)写出下列化学反应方程式
反应②________________________________________________________
反应④_______________________________________________________
反应⑧_______________________________________________________
反应⑩________________________________________________________
(4)写出1mol 物质I与足量的醋酸在浓硫酸加热条件下充分反应生成二元酯的方程式:
_________________________________________________________
写出F与Na2CO3溶液反应的离子方程式:
____________________________________________________________________________
(5)已知物质B在一定条件下可以转变成甲醛,请写出甲醛与银氨溶液反应的离子方程式:
__________________________________________________________
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源.为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4.写出该反应的化学方程式
实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是
(2)测定硫酸铜晶体中结晶水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重;
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重;
步骤5:
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数.
请完成实验步骤5.
(3)已知硫酸铜晶体受热可以逐步失去结晶水,温度升高还可以分解生成铜的氧化物.取25.0g CuSO4?5H2O 晶体均匀受热,缓慢升温至1 200℃并恒温1小时,实验测得固体残留率(
| 剩余固体的质量 | 原始固体质量 |
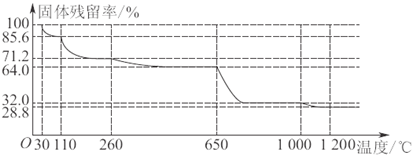
在110℃时所得固体的成分为
在1 200℃并恒温1小时,反应所得气态产物除去水后,物质的量为
A.0mol B.0.1mol C.0.125mol D.大于0.125mol. 查看习题详情和答案>>
(12分)硫酸铜是一种重要的化工原料,工业上常用硫酸为原料来制备硫酸铜。
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源。
①为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4。写出该反应的化学方程式 ;实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是 。
②氯化焙烧工艺是将废渣用氯化钙水溶液调和、成球、高温焙烧,废渣中SiO2与CaCl2等在高温下反应放出HCl,HCl与金属氧化物等反应生成氯化物。反应生成的各金属氯化物以气态形式逸出,进而回收有色金属和回返氯化钙溶液。写出氯化焙烧工艺中生成HCl的化学方程式 。
(2)测定硫酸铜品体中结品水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重:
步骤5: ;
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数。
请完成实验步骤5。
(3)已知硫酸铜品体受热可以逐步失去结品水,温度升高还町以分解生成铜的氧化物。观取25.0g CuSO4·5H2O品体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:
在110℃时所得固体的成分为 ;在1200℃并恒温1小时,反应所得气态产物除去水后,物质的量为 。(填字母)
A.0 mol B.0.1mol C.0.125mol D.大于0.125mol
查看习题详情和答案>>