网址:http://m.1010jiajiao.com/timu3_id_30070[举报]
金属材料在生产生活中应用广泛。
(1)下列用品使用金属材料的是 (填字母序号)。 (2)自然界中的金属大多以化合物形式存在,获取金属单质的方法有多种。工业上用赤铁矿石冶炼铁的化学方程式为 ,这种冶炼方法叫还原法。铝的冶炼多采用电解法,通电分解熔融的氧化铝制取铝的化学方程式为 。
(2)自然界中的金属大多以化合物形式存在,获取金属单质的方法有多种。工业上用赤铁矿石冶炼铁的化学方程式为 ,这种冶炼方法叫还原法。铝的冶炼多采用电解法,通电分解熔融的氧化铝制取铝的化学方程式为 。
(3)珍惜和保护金属资源的措施之一是防止金属锈蚀,使用过的菜刀清洗后需要及时擦干放置,可以减少________对铁锈蚀的影响。
(4)回收废旧金属是保护金属资源的重要措施。化学小组的同学从电子垃圾中获得了含Cu 70%、Al 25%、Fe 4%及少量Au、Pt的电子废料,进行如下回收处理(省略分离操作和部分产品,流程以外的其他产品不含有上述元素)。回答有关问题:
①步骤c在加入固体G前应先除去溶液中的过氧化氢,除去过氧化氢的简单方法用化学方程式表示为 。
②滤液A中含有的溶质是 。
③A~J九种物质中,含有铁元素的是 (填字母序号)。
金属材料在生产生活中应用广泛。
(1)下列用品使用金属材料的是 (填字母序号)。
 (2)自然界中的金属大多以化合物形式存在,获取金属单质的方法有多种。工业上用赤铁矿石冶炼铁的化学方程式为
,这种冶炼方法叫还原法。铝的冶炼多采用电解法,通电分解熔融的氧化铝制取铝的化学方程式为 。
(2)自然界中的金属大多以化合物形式存在,获取金属单质的方法有多种。工业上用赤铁矿石冶炼铁的化学方程式为
,这种冶炼方法叫还原法。铝的冶炼多采用电解法,通电分解熔融的氧化铝制取铝的化学方程式为 。
(3)珍惜和保护金属资源的措施之一是防止金属锈蚀,使用过的菜刀清洗后需要及时擦干放置,可以减少________对铁锈蚀的影响。
(4)回收废旧金属是保护金属资源的重要措施。化学小组的同学从电子垃圾中获得了含Cu 70%、Al 25%、Fe 4%及少量Au、Pt的电子废料,进行如下回收处理(省略分离操作和部分产品,流程以外的其他产品不含有上述元素)。回答有关问题:
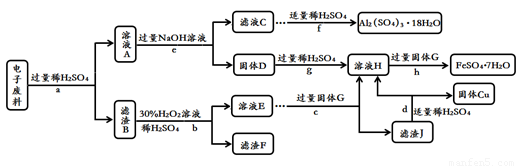
①步骤c在加入固体G前应先除去溶液中的过氧化氢,除去过氧化氢的简单方法用化学方程式表示为 。
②滤液A中含有的溶质是 。
③A~J九种物质中,含有铁元素的是 (填字母序号)。
查看习题详情和答案>>
(1)下列用品使用金属材料的是 (填字母序号)。
 (2)自然界中的金属大多以化合物形式存在,获取金属单质的方法有多种。工业上用赤铁矿石冶炼铁的化学方程式为 ,这种冶炼方法叫还原法。铝的冶炼多采用电解法,通电分解熔融的氧化铝制取铝的化学方程式为 。
(2)自然界中的金属大多以化合物形式存在,获取金属单质的方法有多种。工业上用赤铁矿石冶炼铁的化学方程式为 ,这种冶炼方法叫还原法。铝的冶炼多采用电解法,通电分解熔融的氧化铝制取铝的化学方程式为 。(3)珍惜和保护金属资源的措施之一是防止金属锈蚀,使用过的菜刀清洗后需要及时擦干放置,可以减少________对铁锈蚀的影响。
(4)回收废旧金属是保护金属资源的重要措施。化学小组的同学从电子垃圾中获得了含Cu 70%、Al 25%、Fe 4%及少量Au、Pt的电子废料,进行如下回收处理(省略分离操作和部分产品,流程以外的其他产品不含有上述元素)。回答有关问题:
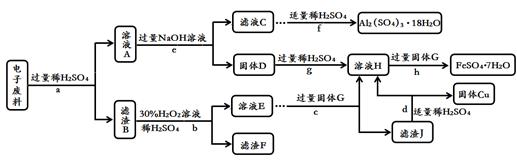
①步骤c在加入固体G前应先除去溶液中的过氧化氢,除去过氧化氢的简单方法用化学方程式表示为 。
②滤液A中含有的溶质是 。
③A~J九种物质中,含有铁元素的是 (填字母序号)。
(1)下列铁制品中,利用金属导热性的是_______(填序号)。


(3)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。实验室制备的方法是:以高纯氮气作保护气,在高温条件下用氢气和氯化亚铁发生置换反应,生成“纳米铁”,反应的化学方程式为_______________________。
(4)氯化铁能腐蚀铜(2FeCl3+Cu==2FeCl2+CuCl2),工业上常用此原理生产印刷线路板。
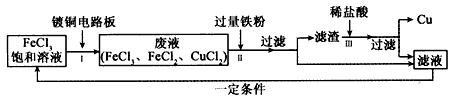
(1)下列应用中使用金属材料的有_________(填字母)。


(3)化学小组收集到洗照片用过的硝酸银废液,利用废铁、废锌回收金属银。他们将金属混合物加入到硝酸银废液中,充分反应后过滤,得到固体和浅绿色溶液(忽略其他杂质),为了探究滤液中溶质的可能组成,他们做出以下猜想:
①溶质为硝酸锌 ②溶质为硝酸亚铁和硝酸银
③溶质为硝酸锌、硝酸亚铁 ④溶质为硝酸锌、硝酸亚铁、硝酸银
上述猜想中正确的是____________。
(4)小组同学继续实验验证所得银粉固体中是否含有铁粉:甲同学用简单的物理方法证明了固体中含有铁粉。他的方法是_____________,乙同学设计了如下测定固体中含银的质量分数的实验步骤:
A.取两药匙样品,加入过量稀硫酸;
B.待充分反应后,取出不溶物;
C.不溶物经洗涤、干燥后称量,记录其质量。
请回答:①步骤B中判断已充分反应的依据是_____________,
②乙同学设计的实验方案能否达到实验目的,请说明理由_______________。