摘要:某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸.其操作为如下几步: ① 用蒸馏水洗涤碱式滴定管.并立即注入NaOH溶液至“0 刻度线以上 ② 固定好滴定管并使滴定管尖嘴充满液体 ③ 调节液面至“0 或“0 刻度线稍下.并记下读数 ④ 移取20.00mL待测液注入洁净的锥形瓶中.并加入3滴酚酞溶液 ⑤ 用标准液滴定至终点.记下滴定管液面读数. 请回答: (1)以上步骤有错误的是 .该错误操作会导致测定结果 (填“偏大 .“偏小 或“无影响 ) (2)步骤⑤中.在记下滴定管液面读数时.滴定管尖嘴有气泡.将导致测定结果(填“偏大 .“偏小 或“无影响 ) (3)判断滴定终点的现象是:锥形瓶中溶液从 色变为 色.且半分钟不变色. (4)图是某次滴定时的滴定管中的液面.其读数为 mL (5)根据下列数据:请计算待测盐酸溶液的浓度: mol/L 滴定次数 待测液体积(mL) 标准烧碱体积(mL) 滴定前读数(mL) 滴定后读数(mL) 第一次 20.00 0.40 20.40 第二次 20.00 4.00 24.00 第二次 20.00 2.00 24.10
网址:http://m.1010jiajiao.com/timu3_id_299274[举报]
 某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管,并直接注入NaOH溶液至“0”刻度线以上
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管,并直接注入NaOH溶液至“0”刻度线以上②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:(1)以上步骤有错误的是(填编号)
①
①
.(2)步骤⑤中,滴定前锥形瓶有少量水,在滴定操作时将导致测定结果(填“偏大”、“偏小”或“无影响”)
无影响
无影响
(3)判断滴定终点的现象是:当滴入最后一滴溶液时,锥形瓶中溶液从无色变为浅红色,且
半分钟内不褪色
半分钟内不褪色
,说明到达终点.(4)图是某次滴定时的滴定管中的液面,其读数为
22.60
22.60
mL(5)根据下列数据:请计算待测盐酸溶液的浓度:
0.2000
0.2000
mol/L| 滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
 某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:(1)以上步骤有错误的是(填编号)
①
①
,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)偏大
偏大
;(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无响”)
偏小
偏小
;(3)判断滴定终点的现象是:锥形瓶中溶液从
无
无
色变为粉红
粉红
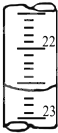
色,且半分钟不变色;(4)右图是某次滴定时的滴定管中的液面,其读数为
22.60
22.60
mL;(5)根据下列数据:请计算待测盐酸溶液的浓度:
0.2000
0.2000
mol/L.| 滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞试液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(2)判断滴定终点的现象是:
(3)如图1是某次滴定时的滴定管中的液面,其读数为

(4)排去碱式滴定管中气泡的方法应采用图2中的
(5)根据下列数据:请计算待测盐酸溶液的浓度:
查看习题详情和答案>>
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞试液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)
①
①
,若测定结果偏高,其原因可能是AD
AD
.A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(2)判断滴定终点的现象是:
锥形瓶中溶液由无色变为浅红色,半分钟不褪色;
锥形瓶中溶液由无色变为浅红色,半分钟不褪色;
.(3)如图1是某次滴定时的滴定管中的液面,其读数为
22.60
22.60
mL.
(4)排去碱式滴定管中气泡的方法应采用图2中的
丙
丙
操作,然后轻轻挤压玻璃球使尖嘴部分充满碱液.(5)根据下列数据:请计算待测盐酸溶液的浓度:
0.2000
0.2000
mol/L.| 滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 2.00 | 21.80 |
| 第三次 | 20.00 | 4.00 | 24.20 |
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管后立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上操作步骤中有一步有错误,请指出编号
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入
(3)下列操作会引起实验结果偏大的是:
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,碱式滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,再用待测液润洗
D.用酸式滴定管量取待测液时将一滴待测液滴在锥形瓶外
(4)判断到达滴定终点的现象是:锥形瓶中溶液从
(5)以下是实验数据记录表
通过计算可得,该盐酸浓度为:
查看习题详情和答案>>
①用蒸馏水洗涤碱式滴定管后立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.

请回答:
(1)以上操作步骤中有一步有错误,请指出编号
①
①
,该错误操作会导致测定结果偏大
偏大
(填“偏大”、“偏小”或“无影响”)(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入
乙
乙
中.(从图中选填“甲”或“乙”)(3)下列操作会引起实验结果偏大的是:
BC
BC
(填编号)A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,碱式滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,再用待测液润洗
D.用酸式滴定管量取待测液时将一滴待测液滴在锥形瓶外
(4)判断到达滴定终点的现象是:锥形瓶中溶液从
无色
无色
色变为浅红
浅红
色,且半分钟之内不再改变.(5)以下是实验数据记录表
| 滴定次数 | 盐酸体积mL | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 16.30 |
| 2 | 20.00 | 0.00 | 16.22 |
0.1626
0.1626
mol?L-1(计算结果保留4位小数). 某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
某学生用0.2000mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管后,立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)
①
①
,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)偏大
偏大
;(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)
偏小
偏小
;(3)判断滴定终点的现象是:锥形瓶中溶液从
无
无
色变为粉红
粉红
色,且半分钟不变色;(4)如图是某次滴定时的滴定管中的液面,其读数为
22.60
22.60
mL;(5)根据下表数据:请计算待测盐酸溶液的浓度为
0.2000
0.2000
mol/L.| 滴定次数 | 待测体积 | 标准烧碱体积 | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第一次 | 20.00 | 4.00 | 24.00 |