摘要:4.洪特规则:电子排布在同一能级的各个轨道时.优先占据不同的轨道.且自旋方向相同.
网址:http://m.1010jiajiao.com/timu3_id_298464[举报]
A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为: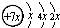 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D的核外电子排布图
 ,这样排布遵循了
,这样排布遵循了
查看习题详情和答案>>
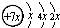 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
Si
Si
BNa
Na
CP
P
DN
N
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
HNO3
HNO3
,碱性最强的是NaOH
NaOH
.(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
F
F
,电负性最大的元素是F
F
.(4)D的氢化物比C的氢化物的沸点
高
高
(填“高“或“低“),原因氨气分子之间含有氢键
氨气分子之间含有氢键
(5)E元素原子的核电荷数是
26
26
,E元素在周期表的第四
四
周期,第Ⅷ
Ⅷ
族,已知元素周期表可按电子排布分为s区、p区等,则E元素在d
d
区.(6)A、B、C最高价氧化物的晶体类型是分别是
原子
原子
晶体、离子
离子
晶体、分子
分子
晶体(7)画出D的核外电子排布图


泡利
泡利
原理和洪特
洪特
规则.高温超导材料是科学家研究的重点物质之一.
(1)科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图1所示.该富勒烯化合物中的K原子和C60分子的个数比为

(2)某同学画出的C的核外电子排布(轨道表示式)如图2所示,该电子排布图(轨道表示式)违背了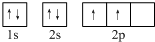
 .
.
(3)金属钾采用的是图3中的
(4)富勒烯(C60)的结构如图4所示.
①1mol C60分子中σ键的数目为
②已知:金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm.有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:
查看习题详情和答案>>
(1)科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图1所示.该富勒烯化合物中的K原子和C60分子的个数比为
3:1
3:1
.
(2)某同学画出的C的核外电子排布(轨道表示式)如图2所示,该电子排布图(轨道表示式)违背了
洪特规则
洪特规则
,请你画出正确的电子排布图(轨道表示式)

(3)金属钾采用的是图3中的
A
A
(填字母代号)堆积方式.(4)富勒烯(C60)的结构如图4所示.
①1mol C60分子中σ键的数目为
90NA
90NA
.②已知:金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm.有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:
错误,因为金刚石是原子晶体,而C60是分子晶体
错误,因为金刚石是原子晶体,而C60是分子晶体
.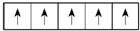 ,而不排布成
,而不排布成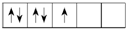 ,其最直接的根据是( )
,其最直接的根据是( ) ,而不排布成
,而不排布成 ,其最直接的根据是( )
,其最直接的根据是( )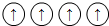 ,而不排成
,而不排成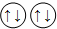 其直接根据是( )
其直接根据是( )