网址:http://m.1010jiajiao.com/timu3_id_297325[举报]
(14分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验:

(1). B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整。
(2).向50毫升18摩/升的H2SO4溶液中加入足量的铜片并加热,充分反应后,
①请写出铜跟浓硫酸反应的化学方程式:_____________________________,写出C中发生反应的离子方程式 。
②被还原的H2SO4的物质的量
A 小于0.45摩 B 等于0.45摩
C 在0.45摩与0.90摩之间 D 大于0.90摩
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是_________ (填写字母编号,有几个写几个,多写或写错0分)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3) 常温下,将铁棒置于浓硫酸中.无明显现象,课本上解释为发生了钝化,但有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面 ,则发生了钝化,若铁棒表面________,则铁和浓硫酸未发生反应。
查看习题详情和答案>>
下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质,B是一种红棕色固体。(反应过程中生成的水及其他产物已略去)
请回答以下问题:
(1)B是 ,H是 ,I是 ,F是 。(填化学式)
(2)写出A和B的反应的化学方程式为 。[来
(3)写出J与D反应转化为G的离子方程式 。
查看习题详情和答案>>
根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是____,在元素周期表中的位置是____________________。
(2)C元素基态原子的电子排布图是下图中的_______(填序号),另一电子排布图不能作为基态原子的电子排布图是因为它不符合_______(从A B C中选择)。
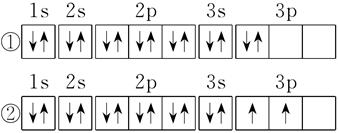
A.能量最低原理 B.泡利原理 C.洪特规则
(3)依据正负化合价代数和等于0,H元素可以放在周期表中的 族
(4)氯化铵的电子式
查看习题详情和答案>>
根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是____,在元素周期表中的位置是____________________。
(2)C元素基态原子的电子排布图是下图中的_______(填序号),另一电子排布图不能作为基态原子的电子排布图是因为它不符合_______(从A B C中选择)。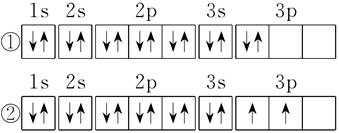
A.能量最低原理 B.泡利原理 C.洪特规则
(3)依据正负化合价代数和等于0,H元素可以放在周期表中的 族
(4)氯化铵的电子式
(14分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验:
(1). B是用来收集实验中产生的气体的装置,但未将导管画全,请直接在原图上把导管补充完整。
(2).向50毫升18摩/升的H2SO4溶液中加入足量的铜片并加热,充分反应后,
①请写出铜跟浓硫酸反应的化学方程式:_____________________________,写出C中发生反应的离子方程式 。
②被还原的H2SO4的物质的量
A 小于0.45摩 B 等于0.45摩
C 在0.45摩与0.90摩之间 D 大于0.90摩
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是_______ __ (填写字母编号,有几个写几个,多写或写错0分)。
__ (填写字母编号,有几个写几个,多写或写错0分)。
| A.铁粉 | B.BaCl2溶液 | C.银粉 | D.Na2CO3溶液 |
 了钝化,若铁棒表面________,则铁和浓硫酸未发生反应。
查看习题详情和答案>>
了钝化,若铁棒表面________,则铁和浓硫酸未发生反应。
查看习题详情和答案>>
