摘要:16.有可逆反应mA(s) + nB(g) pC(g) + qD(g).反应过程中.当其它条件不变时.C的物质的量与温度(T)和压强(P)的关系如图所示.根据图中曲线分析.判断下列叙述中.正确的是 A.到达平衡后.若使用催化剂.C的物质的量增大 B.平衡后.若升高温度.平衡则向逆反应方向移动 C.平衡后增大A的量.有利于提高A的转化率 D.化学方程式中一定是n>p+q 化学试卷 第Ⅰ卷答案栏 总得分表 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu3_id_296739[举报]
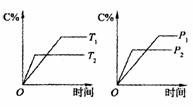
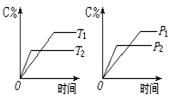
有可逆反应mA(s)+nB(g)![]() pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示:根据图中曲线分析,判断下列叙述中,正确的是
pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示:根据图中曲线分析,判断下列叙述中,正确的是
A.到达平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,平衡则向逆反应 方向移动
C.平衡后增大A的量,有利于提高A的转化率
D.化学方程式中一定![]()
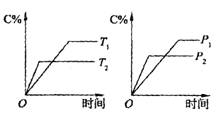
有可逆反应mA(s)+nB(g)![]() pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示:
pC(g)+qD(g),反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图所示:
根据图中曲线分析,判断下列叙述中,正确的是 ( )
A.到达平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,平衡则向逆反应方向移动
C.平衡后增大A的量,有利于提高A的转化率
D.化学方程式中一定![]()
|
可逆反应mA(s)+nB(g)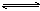 pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是
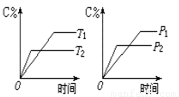
A.到达平衡后,若使用催化剂,C的质量分数增大
B.平衡后,若升高温度,平衡则向逆反应方向移动
C.平衡后,增大A的量,有利于平衡向正反应方向移动
D.化学方程式中一定n>p+q
查看习题详情和答案>>