摘要:22.有两种pH都等于2的酸溶液.一种是强酸.一种是弱酸.现只有石蕊试液.酚酞试液.pH值试纸和蒸馏水.用最简便的方法来鉴别哪瓶是强酸: ①试剂 , ②方法 , ③原理 ,
网址:http://m.1010jiajiao.com/timu3_id_295485[举报]
现有50ml、pH都等于2的四种溶液:①HCl②CH3COOH③HNO3④H2SO4
(1)溶液中含有两种分子的是: (填序号,下同)
(2)加入锌粉,无氢气产生的是
(3)在四种溶液中同时加入同质量的锌粉(足量),经充分与酸反应后,放出氢气最多的是
(4)在与锌完全反应时, 与 消耗锌的质量相同.
(5)分别加入50mlpH=12的NaOH溶液, 反应后溶液的pH最小.
(6) 和 的浓溶液混合后(按一定比例),几乎可溶解所有金属.
查看习题详情和答案>>
(1)溶液中含有两种分子的是:
(2)加入锌粉,无氢气产生的是
(3)在四种溶液中同时加入同质量的锌粉(足量),经充分与酸反应后,放出氢气最多的是
(4)在与锌完全反应时,
(5)分别加入50mlpH=12的NaOH溶液,
(6)
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.工业上常采用NaClO氧化法生产,其生产工艺如下:

主要反应为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH.
(1)写出反应①的离子方程式:
(2)从“混合物II”中分离出K2FeO4后,会有副产品
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.图Ⅰ为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图Ⅱ为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响.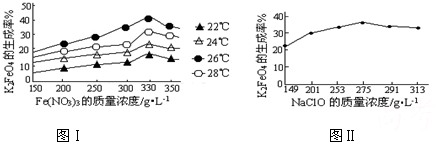
根据图分析:工业生产中最佳温度为
(4)K2FeO4 在水溶液中易水解:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
A.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(5)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0mmol?L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅲ.该实验的目的是
(6)FeO42-在水溶液中的存在形态如图Ⅳ所示.下列说法正确的是
A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O.
查看习题详情和答案>>

主要反应为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O Na2FeO4+2KOH=K2FeO4+2NaOH.
(1)写出反应①的离子方程式:
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.(2)从“混合物II”中分离出K2FeO4后,会有副产品
NaNO3、NaCl、NaOH
NaNO3、NaCl、NaOH
(写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途NaNO3作炸药,NaCl用作调味品或氯碱工业原料等
NaNO3作炸药,NaCl用作调味品或氯碱工业原料等
.(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响.图Ⅰ为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图Ⅱ为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响.

根据图分析:工业生产中最佳温度为
26
26
℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为1.2
1.2
.(4)K2FeO4 在水溶液中易水解:4FeO42-+10H2O
 4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
4Fe(OH)3+8OH-+3O2↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用B
B
溶液(填序号).A.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(5)将适量K2FeO4溶解于pH=4.74的溶液中,配制成c(FeO42-)=1.0mmol?L-1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,测定c(FeO42-)的变化,结果见图Ⅲ.该实验的目的是
探究温度对FeO42-浓度的影响(或其他合理答案)
探究温度对FeO42-浓度的影响(或其他合理答案)
.
(6)FeO42-在水溶液中的存在形态如图Ⅳ所示.下列说法正确的是
C
C
(填字母).A.不论溶液酸碱性如何变化,铁元素都有4种存在形态
B.向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数逐渐增大
C.向pH=6的这种溶液中加KOH溶液,发生反应的离子方程式为:HFeO4-+OH-=FeO42-+H2O.