网址:http://m.1010jiajiao.com/timu3_id_292641[举报]
(2)室温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意,回答下列问题。
①若由0.1 mol·L
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7 mol·L-1
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
查看习题详情和答案>>(1)某研究性学习小组拟用甲醛法测定常见铵态氮肥的含氮量
[资料:4NH4++6HCHO=(CH2)6N4H++3H++6H2O,所生成的H+和(CH2)6N4H+可用NaOH标准溶液滴定,采用酚酞作指示剂]。用甲醛法测定含氮量,不适合的铵盐是__________。(填字母)
a.NH4HCO3 b.(NH4)2SO4 c.NH4Cl
(2)滴定时取待测液于锥形瓶中,操作如下图所示(手持部分省略):正确的操作是图
______,取溶液所用仪器的名称是_________。

反应I:CH3OH(g)→HCHO(g)+H2(g) ΔH1=+92.09kJ/mol,K1=3.92×10-11
反应II:CH3OH(g)+ O2(g)→HCHO(g)+H2O(g) ΔH2=-149.73kJ/mol,
K2=4.35×1029
① 绿色化学提倡化工生产应提高原子利用率。反应________(填“I”或“II”)制甲醛原子利用率更高。从反应的焓变和平衡常数K值看,反应______(填“I”或“II”)制甲醛更加有利。
② 反应Ⅱ自发进行的条件是_________。
a.高温 b.低温 c.任何条件都自发
(4)某研究性学习小组测定居室中甲醛的含量的原理如下,请结合已学知识,
①配平下列方程式:__MnO4- + ___HCHO + ___=___Mn2+ +___CO2↑+_____
②打开a,关闭b,用注射器抽取室内空气;关闭b,打开a,再推动注射器,将气体全部推入酸性KMnO4溶液中,使其充分反应。当B装置中__________时停止推气。若总共取样为500 L空气,则该居室内空气中甲醛的浓度_____________mg/m3。

下列说法不正确的是
A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,![]() 。
。
若加入少量醋酸钠固体,则CH3COOH![]() CH3COO-+H+向左移动,α减小,Ka变小
CH3COO-+H+向左移动,α减小,Ka变小
C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
D.已知:Fe2O3(s)+3C(石墨)![]() 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
CO(g)+![]() O2(g)
O2(g)![]() CO2(g),△H=-283.0 kJ/mol。
CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g)![]() CO2(g),△H=-393.5 kJ/mol。
CO2(g),△H=-393.5 kJ/mol。
则4Fe(s)+3O2(g)![]() 2Fe2O3(s),△H=-1641.0 kJ/mol
2Fe2O3(s),△H=-1641.0 kJ/mol
下列说法不正确的是
A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,。若加入少量醋酸钠固体,则CH3COOH
CH3COO-+H+向左移动,α减小,Ka变小
C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
D.已知:Fe2O3(s)+3C(石墨)2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
CO(g)+1/2O2(g)CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g)CO2(g),△H=-393.5 kJ/mol。
则4Fe(s)+3O2(g)2Fe2O3(s),△H=-1641.0 kJ/mol
查看习题详情和答案>>
下列说法不正确的是
A.已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol 氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
B.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,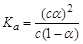 。若加入少量醋酸钠固体,则CH3COOH
。若加入少量醋酸钠固体,则CH3COOH CH3COO-+H+向左移动,α减小,Ka变小
CH3COO-+H+向左移动,α减小,Ka变小
C.实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3916 kJ/mol、-3747 kJ/mol和-3265 kJ/mol,可以证明在苯分子中不存在独立的碳碳双键
D.已知:Fe2O3(s)+3C(石墨) 2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
2Fe(s)+3CO(g),△H=+489.0 kJ/mol。
CO(g)+1/2O2(g) CO2(g),△H=-283.0 kJ/mol。
CO2(g),△H=-283.0 kJ/mol。
C(石墨)+O2(g) CO2(g),△H=-393.5 kJ/mol。
CO2(g),△H=-393.5 kJ/mol。
则4Fe(s)+3O2(g) 2Fe2O3(s),△H=-1641.0 kJ/mol
2Fe2O3(s),△H=-1641.0 kJ/mol
查看习题详情和答案>>