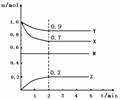
摘要:22.某温度时.在2L的容器中X.Y.Z三种气体的物质的量随着时间的变化曲线如下图所示.下图中数据分析完成下列问题: (1)由图中的数据分析该反应的化学方程式为 (2)前两分钟内.Z的平均反应速率为
网址:http://m.1010jiajiao.com/timu3_id_288972[举报]
某温度时,在2L的容器中X、Y、Z三种气体的物质的量随着时间的变化曲线如下图所示,下图中数据分析完成下列问题:
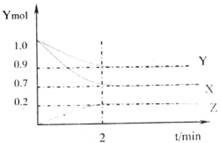
(1)由图中的数据分析该反应的化学方程式为___________________________
(2)前两分钟内,Z的平均反应速率为__________________________________
查看习题详情和答案>> 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析:(1).该反应的化学方程式为
3X+Y 2Z
2Z
 2Z
2Z3X+Y 2Z
2Z
. 2Z
2Z(2).反应开始至2min,用Z表示的平均反应速率为
0.05mol.L-1.min-1
0.05mol.L-1.min-1
.(3).下列叙述能说明上述反应达到平衡状态的是
B、E
B、E
(填序号)A.X、Y、Z的物质的量之比为3:1:2
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗3mol X,同时生成2mol Z
D.混合气体的总质量不随时间的变化而变化
E.混合气体的总物质的量不随时间的变化而变化.
(16分)某温度时,在2L容器中X、Y、Z三种气体物质的量随时间的变化关系曲线如图(2)所示。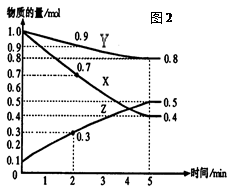
(1)由图中的数据分析,该反应的化学方程式为 。
(2)反应开始至5min,Z的平均反应速率为 ;
(3)反应开始至5min ,正反应速率逐渐 ;逆反应速率逐渐 , 5min后Z的物质的量不再改变,原因是下列的 ;
A.正逆反应都停止了
B.正反应速率为零
C.正逆反应速率相等,反应达到平衡状态
D.逆反应速率为零
(4)下列措施能使正反应速率增大的是
A.升高温度 B.降低温度
C.增大Y的浓度 D.减少Z的浓度
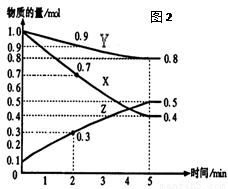
 由图中数据分析:
由图中数据分析: