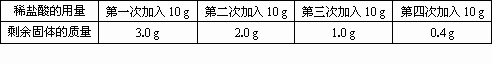网址:http://m.1010jiajiao.com/timu3_id_28857[举报]
| |||||||||||||||||||||||||||
为了测定某石灰石矿样的纯度(其中所含杂质不与酸反应),某同学按如下流程进行实验:
用盐酸溶解矿样→干燥所得气体→用氢氧化钠溶液吸收气体→根据氢氧化钠溶液的增重,计算矿样的纯度
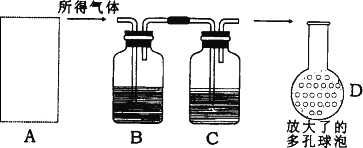
实验装置如图所示,回答下列问题:

(1)A装置为溶解矿样的装置,若已准备了长颈漏斗、双孔橡胶塞、导气管,为了完全溶解矿样,至少还需要的实验仪器是________.
(2)B装置中所盛的试剂是________.
(3)将插入液面的导管下端改成D装置(多孔球泡),有利于提高实验的准确度,其理由是________.
| |||||||||||||||


(1)A为溶解矿样的装置,若已经准备了长颈漏斗、双孔橡胶塞、导气管,为了完成溶解至少还需要的实验仪器是
(2)A中发生反应化学方程式
(3)B中所盛的试剂是
(4)根据上述装置进行实验,下列情况会使实验结果产生偏差的是
①实验开始A、B装置以及导气管内残留有少量空气
②进入C装置的气体中还混有少量HCl气体
③气体通过速度过快,CO2来不及被NaOH溶液全部吸收
④实验结束时,系统内还残留有少量CO2气体
(5)将插入溶液的管子的下端改成具有多孔的球泡(图中的D),有利于提高实验的准确度,其理由是
(6)改进实验装置并进行正确操作可以准确测出矿样的纯度,若此时C装置在实验前后其质量增加了3.6 g,则该矿样的纯度为