摘要:与CH2=CH2 ® CH2Br-CH2Br的变化属于同一反应类型的是 A.CH3CHO ® C2H5OH B.C2H5Cl ® CH2=CH2 C. D.CH3COOH ® CH3COOC2H5
网址:http://m.1010jiajiao.com/timu3_id_285202[举报]
如图中A、B、C、D、E、F、G均为有机化合物.
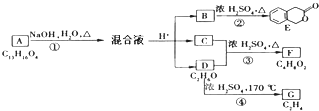
根据上图回答问题:
(1)D的化学名称是 .
(2)反应③的化学方程式是 .(有机物须用结构简式表示)
(3)B的分子中官能团的名称 .A的结构简式是 .反应①的反应类型是 .
(4)符合下列3个条件的B的同分异构体的数目有 个.
①含有邻二取代苯环结构;②与B有相同官能团;③不与FeCl3溶液发生显色反应写出其中任意一个同分异构体的结构简式 .
(5)已知:R-CH=CH2
R-CH2-CH2-Br请设计合理方案从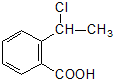 合成
合成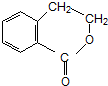 (用反应流程图表示,并注明反应条件) .
(用反应流程图表示,并注明反应条件) .
例:由乙醇R-CH=CH2
R-CH2-CH2-Br合成聚乙烯的反应流程图可表示为:
CH3CH2OH
CH2=CH2
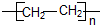
查看习题详情和答案>>

根据上图回答问题:
(1)D的化学名称是
(2)反应③的化学方程式是
(3)B的分子中官能团的名称
(4)符合下列3个条件的B的同分异构体的数目有
①含有邻二取代苯环结构;②与B有相同官能团;③不与FeCl3溶液发生显色反应写出其中任意一个同分异构体的结构简式
(5)已知:R-CH=CH2
| HBr |
| 过氧化物 |
 合成
合成 (用反应流程图表示,并注明反应条件)
(用反应流程图表示,并注明反应条件)例:由乙醇R-CH=CH2
| HBr |
| 过氧化物 |
CH3CH2OH
| 浓H2SO4 |
| 170℃ |
| 高温高压 |
| 催化剂 |
铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁.“速力菲”是市场上一种常见的补铁药物,下列表格是它的说明书:

(1)该药品中Fe2+会缓慢氧化,国家规定该药物中Fe2+的氧化率超过10%即不能再服用.
①为了检验某药店出售的“速力菲”是否被氧化,实验室可选用的最常用最灵敏的检验试剂为
②实验室采用H2SO4酸化的KMnO4溶液对“速力菲”中的Fe2+进行滴定(假设药品中其他成分不与KMnO4反应).离子方程式如下:aMnO
+bFe2++cH+═dMn2++eFe3++fH2O,当a=1时,b=
③称量上述含铁元素质量分数为20.00%的“速力菲”10.00g,将其全部溶于稀硫酸中,配制成1 000.00mL溶液.取出20.00mL,用0.01mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL.该药品可以服用吗?
(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸.含23.6g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和.质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子.写出琥珀酸溶液与氢氧化钠溶液完全中和的化学方程式(有机物须写结构简式):
查看习题详情和答案>>

(1)该药品中Fe2+会缓慢氧化,国家规定该药物中Fe2+的氧化率超过10%即不能再服用.
①为了检验某药店出售的“速力菲”是否被氧化,实验室可选用的最常用最灵敏的检验试剂为
硫氰化钾溶液
硫氰化钾溶液
(填试剂的名称).②实验室采用H2SO4酸化的KMnO4溶液对“速力菲”中的Fe2+进行滴定(假设药品中其他成分不与KMnO4反应).离子方程式如下:aMnO
- 4 |
5
5
.③称量上述含铁元素质量分数为20.00%的“速力菲”10.00g,将其全部溶于稀硫酸中,配制成1 000.00mL溶液.取出20.00mL,用0.01mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL.该药品可以服用吗?
不可以
不可以
(填“可以”或“不可以”),请通过计算简述理由:由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01 mol/L×12.00×10-3L×5×
=0.03 mol,
m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率:
=16.00%>10%,所以不可以服用
| 1000.00 mL |
| 20.00 mL |
m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率:
| 10 g×20.00%-1.68 g |
| 10 g×20.00% |
由MnO4-~5Fe2+,可得1000.00mL溶液含有的Fe2+的物质的量n(Fe2+)=0.01 mol/L×12.00×10-3L×5×
=0.03 mol,
m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率:
=16.00%>10%,所以不可以服用
(写出主要计算过程).| 1000.00 mL |
| 20.00 mL |
m(Fe2+)=0.03 mol×56 g/mol=1.68 g,Fe2+的氧化率:
| 10 g×20.00%-1.68 g |
| 10 g×20.00% |
(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸.含23.6g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和.质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子.写出琥珀酸溶液与氢氧化钠溶液完全中和的化学方程式(有机物须写结构简式):
HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O
HOOC-CH2-CH2-COOH+2OH-→-OOC-CH2-CH2-COO-+2H2O
;琥珀酸亚铁的化学式为FeC4H4O4
FeC4H4O4
.
现有下列各化合物:
A.
B.
C.
D.CH3CH2C≡CH与CH2═CH-CH═CH2
(1)上述化合物中的含氧官能团是(至少写出两个名称) ;
(2)B中的两种氨基酸混合生成的二肽最多有 种:
(3)鉴别C中的两种有机物可选用的试剂为 .
(4)写出CH2═CH-CH═CH2发生聚合反应的化学方程式 .
(5)上述化合物中属于同分异构体的是 ,属于同系物的是 (填字母代号).
查看习题详情和答案>>
A.

B.

C.

D.CH3CH2C≡CH与CH2═CH-CH═CH2
(1)上述化合物中的含氧官能团是(至少写出两个名称)
(2)B中的两种氨基酸混合生成的二肽最多有
(3)鉴别C中的两种有机物可选用的试剂为
(4)写出CH2═CH-CH═CH2发生聚合反应的化学方程式
(5)上述化合物中属于同分异构体的是
与CH2=CH2→CH2Br-CH2Br的变化属于同一反应类型的是( )
| A、CH3CHO→C2H5OH | B、C2H5Cl→CH2=CH2 | C、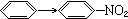 | D、CH3COOH→CH3COOC2H5 |
有下列3种有机化合物A:CH2=CH2、B: 、C:CH3COOH
、C:CH3COOH
(1)写出化合物A、C中官能团的名称
(2)3种化合物中能使溴的四氯化碳溶液褪色的是
 (写结构简式).
(写结构简式).
(3)3种化合物中能与乙醇发生酯化反应的是
反应类型为:
查看习题详情和答案>>
 、C:CH3COOH
、C:CH3COOH(1)写出化合物A、C中官能团的名称
碳碳双键
碳碳双键
、羧基
羧基
;(2)3种化合物中能使溴的四氯化碳溶液褪色的是
乙烯
乙烯
(写名称);反应的化学方程式为:CH2=CH2+Br2→CH2Br-CH2Br
CH2=CH2+Br2→CH2Br-CH2Br
;具有特殊气味、常做有机溶剂的是

(3)3种化合物中能与乙醇发生酯化反应的是
乙酸
乙酸
(写名称);反应的化学方程式为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
| 浓H2SO4 |
| △ |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
;| 浓H2SO4 |
| △ |
反应类型为:
酯化反应
酯化反应
.