摘要:9.M2O7x-离子和S2-在酸性条件下发生如下反应:M2O7x-+3 S2-+14H+=2M3++3S↓+7H2O.则M2O7x-离子中M的化合价是 .
网址:http://m.1010jiajiao.com/timu3_id_285100[举报]
Ⅰ. 已知某工业废水中含有大量的CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其他物质.

(1)步骤1需用到的玻璃仪器除烧杯外有
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
(3)步骤3中涉及的操作是:蒸发浓缩、
(4)步骤2应该在通风橱中进行,原因是
Ⅱ.((2)为1分,其余每空2分)某溶液中含有Na+、SO42-、SO32-、CO32-、Cl-、Br-中的若干种,依次进行下列实验,观察到的现象记录如下:①加入盐酸,有无色气体生成;②向原溶液中滴加氯水,无气体产生,再加CCl4振荡,静置,CCl4层呈橙色,用分液漏斗分液;③向分液后所得的水溶液中加入Ba(NO3)2和HNO3的混合溶液,有白色沉淀生成,过滤;④在滤液中加AgNO3和HNO3的混合液,有白色沉淀产生.试回答:(提示:氯气会氧化SO32-为SO42-)
(1)原溶液中肯定存在的离子是
(2)若步骤③改用BaCl2和盐酸的混合溶液,对判断(1)结论有无影响
(3)步骤②中发生反应的离子方程式为
查看习题详情和答案>>

(1)步骤1需用到的玻璃仪器除烧杯外有
漏斗、玻璃棒
漏斗、玻璃棒
.(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
Cu
Cu
,固体残渣的成分是(填化学式)Ag、Cu
Ag、Cu
.(3)步骤3中涉及的操作是:蒸发浓缩、
冷却结晶
冷却结晶
、过滤、烘干.(4)步骤2应该在通风橱中进行,原因是
因为Hg有挥发性,且有毒
因为Hg有挥发性,且有毒
.Ⅱ.((2)为1分,其余每空2分)某溶液中含有Na+、SO42-、SO32-、CO32-、Cl-、Br-中的若干种,依次进行下列实验,观察到的现象记录如下:①加入盐酸,有无色气体生成;②向原溶液中滴加氯水,无气体产生,再加CCl4振荡,静置,CCl4层呈橙色,用分液漏斗分液;③向分液后所得的水溶液中加入Ba(NO3)2和HNO3的混合溶液,有白色沉淀生成,过滤;④在滤液中加AgNO3和HNO3的混合液,有白色沉淀产生.试回答:(提示:氯气会氧化SO32-为SO42-)
(1)原溶液中肯定存在的离子是
Na+、SO32-、Br-
Na+、SO32-、Br-
,肯定没有的离子是CO32-
CO32-
;(2)若步骤③改用BaCl2和盐酸的混合溶液,对判断(1)结论有无影响
无影响
无影响
;(3)步骤②中发生反应的离子方程式为
Cl2+2Br-═Br2+2Cl-
Cl2+2Br-═Br2+2Cl-
、Cl2+SO32-+H2O═2Cl-+SO42-+2H+
Cl2+SO32-+H2O═2Cl-+SO42-+2H+
.(I)按照如图1所示装置进行有关实验,拔掉分液漏斗玻璃塞,将A逐滴加入B中.
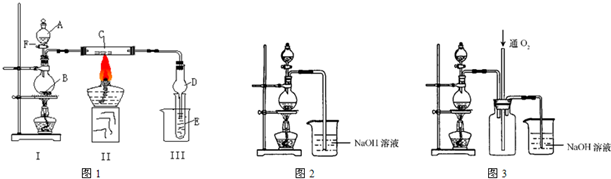
若A是浓盐酸,B为二氧化锰,当将A滴入B中时发生反应的离子方程式为:
当实验一段时间后,发现C、D中有红棕色烟,则C的化学式为:
(II)硫酸铜是一种应用极其广泛的化工原料,可通过多种途径制取硫酸铜晶体.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图2所示).
请回答相关问题:
(1)图2分液漏斗中装的液体是
(2)本实验中若硝酸过量,造成的结果是
(3)图3是图2的改进装置,其优点是①
(4)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:将铜粉在某仪器中反复灼烧,使铜粉与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向混合物中加入Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,得硫酸铜晶体,滤渣循环使用〔已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4〕.
①方案1中用于灼烧铜粉的仪器名称是
②方案2中甲物质可以是
a.CuO b.CuCO3 c.CaCO3 d.NaOH
③方案2中发生反应的总化学方程式为(注明反应条件)
查看习题详情和答案>>

若A是浓盐酸,B为二氧化锰,当将A滴入B中时发生反应的离子方程式为:
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
;
| ||
当实验一段时间后,发现C、D中有红棕色烟,则C的化学式为:
Fe
Fe
.(II)硫酸铜是一种应用极其广泛的化工原料,可通过多种途径制取硫酸铜晶体.铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图2所示).
请回答相关问题:
(1)图2分液漏斗中装的液体是
浓硝酸
浓硝酸
;(2)本实验中若硝酸过量,造成的结果是
制得的硫酸铜晶体不纯
制得的硫酸铜晶体不纯
;(3)图3是图2的改进装置,其优点是①
有利于氮氧化合物的吸收
有利于氮氧化合物的吸收
,②防止倒吸
防止倒吸
;(4)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:将铜粉在某仪器中反复灼烧,使铜粉与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应.
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向混合物中加入Fe2(SO4)3,即发生反应.反应完全后向其中加物质甲调节pH到3~4,产生Fe(OH)3沉淀,过滤、蒸发、结晶,得硫酸铜晶体,滤渣循环使用〔已知Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为3.7、6.4〕.
①方案1中用于灼烧铜粉的仪器名称是
坩埚
坩埚
;②方案2中甲物质可以是
ab
ab
(填字母序号);a.CuO b.CuCO3 c.CaCO3 d.NaOH
③方案2中发生反应的总化学方程式为(注明反应条件)
2Cu+O2+2H2SO4
2CuSO4+2H2O
| ||
2Cu+O2+2H2SO4
2CuSO4+2H2O
.
| ||
现有下列物质,用编号填空回答下列问题:(每空各2分多选错选不得分)
A.干冰 B.金刚石 C.氩 D.过氧化钠 E.二氧化硅 F.溴化铵
(1)通过非极性键形成的原子晶体是:
(2)可由原子直接构成的分子晶体是:
(3)含有离子键、共价键、配位键的化合物是:
(4)含有非极性键的离子化合物是:
查看习题详情和答案>>
A.干冰 B.金刚石 C.氩 D.过氧化钠 E.二氧化硅 F.溴化铵
(1)通过非极性键形成的原子晶体是:
B
B
.(2)可由原子直接构成的分子晶体是:
C
C
.(3)含有离子键、共价键、配位键的化合物是:
F
F
.(4)含有非极性键的离子化合物是:
D
D
.如图是部分元素的单质和化合物之间的相互转化关系,部分反应的生成物没有全部列出.已知原料A、M均属于金属氧化物,L是由两种沉淀组成的.F和Y反应能生成一种全部为非金属元素所组成的盐,C的焰色反应呈黄色,M有磁性,反应①中B和C的物质的量之比为3:4.
回答下列问题:
(1)反应②的主要用途是:
(2)已知反应③中还有一种无色气体生成,写出反应③的离子方程式:
(3)L中两种沉淀为
(4)若将M溶于稀硫酸中可形成溶液Z,请设计简单的实验,证明Z溶液中所含的金属阳离子:

查看习题详情和答案>>
回答下列问题:
(1)反应②的主要用途是:
冶炼金属或焊接钢轨
冶炼金属或焊接钢轨
(答一点即可,2分),Y的空间构型为三角锥型
三角锥型
.(2)已知反应③中还有一种无色气体生成,写出反应③的离子方程式:
3Fe3O4+28H++NO3-=9Fe3++NO+14H2O
3Fe3O4+28H++NO3-=9Fe3++NO+14H2O
.(3)L中两种沉淀为
Fe(OH)3、Al(OH)3
Fe(OH)3、Al(OH)3
(用化学式表示),A的化学式为Na2O2
Na2O2
.(4)若将M溶于稀硫酸中可形成溶液Z,请设计简单的实验,证明Z溶液中所含的金属阳离子:
分别取少量乙溶液于两支洁净的试管中,向第一支试管中滴加硫氰化钾溶液,溶液变血红色,证明有Fe3+,向第二只试管中,滴加少量酸性高锰酸钾溶液,振荡,高锰酸钾紫色褪去,证明含有Fe2+
分别取少量乙溶液于两支洁净的试管中,向第一支试管中滴加硫氰化钾溶液,溶液变血红色,证明有Fe3+,向第二只试管中,滴加少量酸性高锰酸钾溶液,振荡,高锰酸钾紫色褪去,证明含有Fe2+
.