摘要:2.将1mol下列物质:①Na2O. ②NaOH.③Na2O2.④Na2SO3.⑤Na.长期放置于空气中. 最后质量增加的情况是 A.①=②>③>④>⑤ B.①>⑤>③>④>② C.②=⑤>①=③>④ D.④>②>③>⑤>①
网址:http://m.1010jiajiao.com/timu3_id_284948[举报]
 (2010?漳州二模)[化学---物质结构与性质]研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.
(2010?漳州二模)[化学---物质结构与性质]研究物质的微观结构,有助于人们理解物质变化的本质.请回答下列问题.(1)P、S、Cl三种元素中,第一电离能最小的是
S
S
.(2)PCl3和CH4中心原子的杂化类型相同,PCl3分子的空间构型是
三角锥形
三角锥形
.(3)钛原子的电子排布式为
1s22s22p63s23p63d24s2
1s22s22p63s23p63d24s2
.在浓的TiCl3溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3?6H2O的绿色晶体,将1mol该物质溶于水,加入足量硝酸银溶液,立即产生1mol氯化银沉淀,则该配合物阳离子的化学式为[TiCl2(H2O)4]+
[TiCl2(H2O)4]+
,形成该离子时提供孤电子对的分子或离子是H2O、Cl-
H2O、Cl-
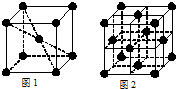
(填化学式).(4)铁元素在1183K以下形成的晶体的基本结构单元如图1所示,1183K以上转变为图2所示结构的基本结构单元.两种晶体的基本结构单元中的原子个数之比为
1:2
1:2
.(8分)、钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有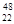 Ti和
Ti和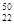 Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;按电子排布Ti元素在元素周期表分区中属于 (填s、p、d、ds或f)区元素
Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 周期,第 族;按电子排布Ti元素在元素周期表分区中属于 (填s、p、d、ds或f)区元素
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡为离子晶体,晶胞的结构如右图所示,它的化学式是 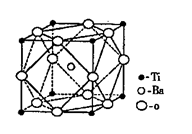
(3)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为1mol,已知该配合物的配位数为6,则该配合物的配位体是 。
1mol该配合物外界所含结晶水物质的量为 mol。