摘要:6.一定条件下的密闭容器中.进行如下反应NO N2(g)+CO2(g).△H﹤0.达到平衡后.为提高该反应的反应速率和NO的转化率.采取的措施正确的是 ( ) A.加催化剂同时升高温度 B.加催化剂同时增大压强 C.升高温度同时充入N2 D.降低温度同时增大压强
网址:http://m.1010jiajiao.com/timu3_id_283809[举报]
一定条件下的密闭容器中,进行如反应:NO(g)+CO(g)
N2(g)+CO2(g);△H=-373.2kJ/mol
为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是( )
| 1 |
| 2 |
为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是( )
| A、加(正)催化剂 |
| B、增大压强(体积减小) |
| C、给体系加热 |
| D、从体系中不断移去部分CO2 |
一定条件下的密闭容器中,进行如下反应:NO(g)+CO(g)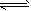 N2(g)+CO2(g) ΔH=-373.2 kJ/mol 为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是
N2(g)+CO2(g) ΔH=-373.2 kJ/mol 为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是
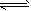 N2(g)+CO2(g) ΔH=-373.2 kJ/mol 为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是
N2(g)+CO2(g) ΔH=-373.2 kJ/mol 为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是 [ ]
A.加(正)催化剂
B.增大压强(体积减小)
C.给体系加热
D.从体系中不断移去部分CO2
查看习题详情和答案>>
B.增大压强(体积减小)
C.给体系加热
D.从体系中不断移去部分CO2
(14分)密闭容器中,保持一定温度,进行如下反应:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
已知加入1mol N2和3mol H2,在恒压条件下,达到平衡时生成amol NH3[见下表中编号(1)的一行];在恒容条件下,达到平衡时生成b mol NH3[见下表中编号(4)的一行]。若相同条件下,达到平衡时混合物中各组分的百分含量不变,请填空:![]()
状状 条件 | 起始时各物的物质的量(mol) | 平衡时NH3的物质的量 (mol) | ||||
编号 | x(N2) | y(H2) | z(NH3) | |||
恒
压 | (1) | 1 | 3 | 0 | a | |
(2) | 3 |
| 0 |
| ||
(3) |
|
| 0.2 | 0.5a | ||
x、y、z取值必须满足的一般条件: 。 | ||||||
恒
容 | (4) | 1 | 3 | 0 | b | |
(5) | 0 | 0 |
| b | ||
(6) |
| 2.25 |
| b | ||
x、y、z取值必须满足一般条件(一个只含x、z,另一个只含y、z): ; 。 | ||||||
| a与b的关系是:a b(填>、<、=) | |||||
查看习题详情和答案>>
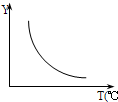 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表,回答下列问题:
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g).其化学平衡常数K和温度T的关系如下表,回答下列问题:| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
>
>
0;若该反应符合如图所示的关系,则在图中,Y轴是指CO2或H2的百分含量等
CO2或H2的百分含量等
. (答出一种即可)(2)能判断该反应达到化学平衡状态的依据是
bc
bc
(多选扣分).a.容器中压强不变 b.混合气体中c(CO)不变
c.v(H2)正=v(H2O)逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:0.9?c(CO2)?c(H2)=c(CO)?c(H2O),由此可以判断此时的温度为
800
800
℃.其它条件不变,升高温度,原化学平衡向逆
逆
反应方向移动(填“正”或“逆”),容器内混合气体的平均相对分子质量不变
不变
(填“增大”、“减小”或“不变”).