摘要:20.(重)一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧 化碳.该电池负极发生的反应是 A.CH30H(g)+O2(g)=H2O(1)+CO2(g)+2H+(aq)+2e B.O 2(g)+4H+(aq)+4e =2H20(1) C.O2(g)+2H2O(1)+4e =40H D.CH30H(g)+H2O-6e (1)=CO2 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu3_id_283546[举报]
由于燃料电池汽车,尤其氢燃料电池汽车可以实现零污染排放,驱动系统几乎无噪音,且氢能取之不尽、用之不竭,燃料电池汽车成为近年来汽车企业关注的焦点.为了获得竞争优势,各国纷纷出台政策,加速推进燃料电池关键技术的研发.燃料电池的燃料有氢气、甲醇、汽油等.
(1)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料.已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2 (g)=2H2O (l)△H=-571.6kJ?mol-1 ①
CH3OH(l)+O2(g)→CO2(g)+2H2O(l)△H=-726.0kJ?mol-1 ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:
(2)有科技工作者利用稀土金属氧化物作为固体电解质制造出了甲醇一空气燃料电池.这种稀土金属氧化物在高温下能传导O2-.
①电池正极发生的反应是
负极发生的反应是
②在稀土金属氧化物的固体电解质中,O2-的移动方向是
③甲醇可以在内燃机中燃烧直接产生动力推动机动车运行,而科技工作者却要花费大量的精力研究甲醇燃料汽车.主要原因是:
查看习题详情和答案>>
(1)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料.已知氢气、甲醇燃烧的热化学方程式如下:
2H2(g)+O2 (g)=2H2O (l)△H=-571.6kJ?mol-1 ①
CH3OH(l)+O2(g)→CO2(g)+2H2O(l)△H=-726.0kJ?mol-1 ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:
CO2 (g)+3H2 (g)=CH3OH(l)+H2O (l)△H=-131.4 kJ?mol-1
CO2 (g)+3H2 (g)=CH3OH(l)+H2O (l)△H=-131.4 kJ?mol-1
.(2)有科技工作者利用稀土金属氧化物作为固体电解质制造出了甲醇一空气燃料电池.这种稀土金属氧化物在高温下能传导O2-.
①电池正极发生的反应是
O2+4e-=2O2-
O2+4e-=2O2-
;负极发生的反应是
CH2OH+4O2--8e-=CO2+2H2O
CH2OH+4O2--8e-=CO2+2H2O
.②在稀土金属氧化物的固体电解质中,O2-的移动方向是
从正极流向负极
从正极流向负极
.③甲醇可以在内燃机中燃烧直接产生动力推动机动车运行,而科技工作者却要花费大量的精力研究甲醇燃料汽车.主要原因是:
燃料电池的能量转化率高
燃料电池的能量转化率高
.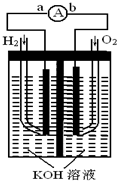 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:(1)氢氧燃料电池的能量转化主要形式是
化学能转变为电能
化学能转变为电能
,在导线中电子流动方向为由a到b
由a到b
(用a、b表示).(2)负极反应式为
2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
.(3)电极表面镀铂粉的原因为
增大电极单位面积吸附H2、O2分子数?加快反应速率
增大电极单位面积吸附H2、O2分子数?加快反应速率
.(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2
| ||
Ⅱ.LiH+H2O═LiOH+H2↑
①反应Ⅰ中的还原剂是
Li
Li
,反应Ⅱ中的氧化剂是水
水
.②用锂吸收224L(标准状况)H2,生成的LiH与H2O作用后放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
32
32
mol.(5)肼一空气燃料电池是一种碱性电池,该电池放电时,肼作
负
负
极,其电极反应式为(生成无污染物质)N2H4-4e-+4OH-═N2+4H2O
N2H4-4e-+4OH-═N2+4H2O
.运用化学反应原理研究碳的氧化物的性质具有重要意义.
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高.下列措施不能够有效控制CO2所导致的温室效应的是
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka=4.7×10-8.写出84消毒液露置在空气中发生反应的离子方程式
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应.
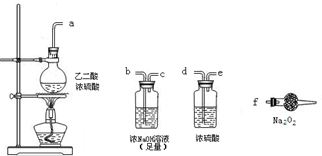
已知:H2C2O4
CO2↑+CO↑+H2O,则实验选择的最简单的装置接口连接顺序为
(4)已知C(s)+O2(g)=CO2(g),△H=-393.5kJ?mol-1;CO(g)+
O2(g)=CO2(g),△H=-283.0kJ?mol-1,写出CO2 和C(s)反应的热化学方程式
查看习题详情和答案>>
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高.下列措施不能够有效控制CO2所导致的温室效应的是
④
④
(填序号)①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka=4.7×10-8.写出84消毒液露置在空气中发生反应的离子方程式
ClO-+CO2+H2O=HClO+HCO3-;2HClO=2H++2Cl-+O2↑
ClO-+CO2+H2O=HClO+HCO3-;2HClO=2H++2Cl-+O2↑
.(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应.

已知:H2C2O4
| ||
| △ |
abcf
abcf
;若CO能够与Na2O2发生反应,则预测反应产物为Na2CO3
Na2CO3
.(4)已知C(s)+O2(g)=CO2(g),△H=-393.5kJ?mol-1;CO(g)+
| 1 |
| 2 |
CO2(g)+C(s)=2CO(g)△H=+172.5kJ?mol-1
CO2(g)+C(s)=2CO(g)△H=+172.5kJ?mol-1
.以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为CO+CO32-→2CO2+2e-
CO+CO32-→2CO2+2e-
.若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)11.2
11.2
L.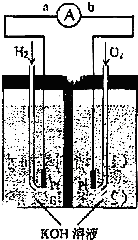 氢氧燃料电池是符合绿色化学理念的新型发电装置.图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答:(1)氢氧燃料电池的能量转化主要形式是
(2)负极反应式为
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一,金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2
| ||
Ⅱ.LiH+H2O═LiOH+H2↑
①反应Ⅰ中的还原剂是
②已知LiH固体密度为 0.82g/cm3.用锂吸收 224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
③由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
![]()
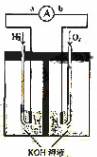
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
![]() (2)负极反应式为 。
(2)负极反应式为 。
![]() (3)电极表面镀铂粉的原因为 。
(3)电极表面镀铂粉的原因为 。
![]() (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
![]() Ⅰ.2Li+H2
Ⅰ.2Li+H2![]()
![]() 2LIH
2LIH
![]() Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
![]() ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
查看习题详情和答案>>