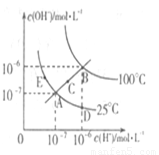
摘要:水的电离平衡如右图所示. (1)若A点表示25℃时水的电离平衡状态.当升高温度至100℃时水的电离平衡状态为B点.则此时水的离子积为 . (2)将100℃时pH=8的Ba(OH)2溶液与pH=5的盐酸混合.并保持100℃的恒温.欲使混合溶液的pH=7.则Ba(OH)2溶液与盐酸的体积比为 . (3)已知AnBm的离子积=c(Am+)n•c(Bn-)m,若某温度下Ca(OH)2的溶解度为0.74g,其饱和溶液的密度为1g/mL,其离子积为 .
网址:http://m.1010jiajiao.com/timu3_id_282927[举报]
水的电离平衡曲线如右图所示,下列说法不正确的是 ( )
A.图中五点Kw间的关系:B>C>A=D=E
B.若从A点到D点,可采用在水中加入少量酸的方法
C.若从A点到C点,可采用温度不变时在水中加入适量NH4C1固体的方法
D.若处在B点时,将pH =2的硫酸溶液与pH = 10的KOH溶液等体积混合,所得溶液呈中性
查看习题详情和答案>>
水的电离平衡曲线如右图所示,下列说法不正确的是 ( )
A.图中五点Kw间的关系:B>C>A=D=E
B.若从A点到D点,可采用在水中加入少量酸的方法
C.若从A点到C点,可采用温度不变时在水中加入适量NH4C1固体的方法
D.若处在B点时,将pH =2的硫酸溶液与pH = 10的KOH溶液等体积混合,所得溶液呈中性
查看习题详情和答案>>
 水的电离平衡曲线如右图所示,下列说法不正确的是( )
水的电离平衡曲线如右图所示,下列说法不正确的是( )