摘要:11.化学探究活动或化学探究实验.要尽可能的对实验前.实验中.实验后三个阶段进行观察.观察的主要内容是: (1)物质的性质.如 . . . . . . 等, (2)物质发生的 .如是否发生熔化.发光.放热.生成气体等, (3)关注物质的变化过程及现象.对物质变化的 . . 三个阶段的现象进行仔细的观察和描述.通过分析比较.得出实验结论. 答案:(1)颜色 状态 气味 硬度 密度 熔点 沸点 变化前 变化中 变化后 能力提高
网址:http://m.1010jiajiao.com/timu3_id_28268[举报]
化学探究活动或化学探究试验,要尽可能地对实验前、实验中、实验后三个阶段进行观察,观察的主要内容是:
(1)物质的性质,如________、________、________、________、________、________、________等;
(2)物质发生的________,如是否发生熔化、发光、放热、生成气体等;
(3)物质的变化过程及现象,对物质变化的________、________、________三个阶段的现象进行仔细地观察和描述,通过分析比较,得出实验结论.
查看习题详情和答案>>某化学探究活动小组的小峰同学为了测定某不纯氧化铁试样(其中的杂质不参与反应)中氧化铁的质量分数,设计了如图所示的实验装置.(注:3H2+Fe2O3 2Fe+3H2O)
2Fe+3H2O)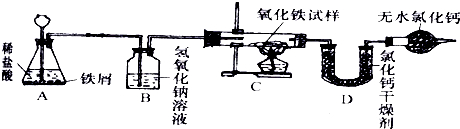
试回答下列问题:
(1)写出A中发生反应的化学方程式:______.
(2)若已知C中玻璃管的质量为100g,并称量了以下相关数据:
| 质量g | 反应前 | 反应后 |
| ①C中玻璃管与样品质量 | 120g | 115.2g |
| ②D中U型管与干燥剂质量 | 200g | 206g |
实验室制取气体时,常用到如下图所示的装置.某兴趣小组的同学要利用所给装置进行以下探究学习活动,请你一同参加并回答下列问题.
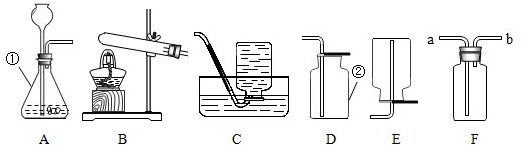
(1)写出标号仪器的名称:①
(2)明明要用A装置制取氧气,请写出该反应的化学方程式
(3)伟伟要用高锰酸钾制取较纯净的氧气,反应的化学方程式为
(4)强强认为,F装置既能收集气体还能干燥气体.他要用排水法来收集氧气,就在广口瓶里装满水,让气体应从
(5)彤彤依上图选用了适当装置,成功地制得了二氧化碳.他选用的制取装置由
(6)佳佳要检验彤彤制得的气体就是二氧化碳,便在F装置中加入试剂
查看习题详情和答案>>

(1)写出标号仪器的名称:①
锥形瓶
锥形瓶
; ②集气瓶
集气瓶
.(2)明明要用A装置制取氧气,请写出该反应的化学方程式
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(3)伟伟要用高锰酸钾制取较纯净的氧气,反应的化学方程式为
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.他应选择的制取装置有
| ||
BC
BC
.该装置存在不足之处,可能会导致高锰酸钾小颗粒进入导气管
高锰酸钾小颗粒进入导气管
.(4)强强认为,F装置既能收集气体还能干燥气体.他要用排水法来收集氧气,就在广口瓶里装满水,让气体应从
b
b
(填“a”或“b”)端通入;他要干燥氧气,便在广口瓶里盛装适量浓硫酸
浓硫酸
,让气体从a端通入b端导出.(5)彤彤依上图选用了适当装置,成功地制得了二氧化碳.他选用的制取装置由
AD
AD
组成,最佳反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(6)佳佳要检验彤彤制得的气体就是二氧化碳,便在F装置中加入试剂
石灰水
石灰水
,将气体由a通入,此时广口瓶内发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
.但佳佳的实验并没有产生预期的现象.当彤彤和佳佳都确认各自所用试剂没有变质或失效时.请帮他们找出导致此结果的可能的原因收集的二氧化碳中混有氯化氢气体
收集的二氧化碳中混有氯化氢气体
.化学小组同学对于“金属和硫酸反应的快慢与什么因素有关”的课题开展探究
【已有知识】
(1)根据金属的活动性顺序,只有排在氢(H)前面的金属才能与稀盐酸或稀硫酸反应制取氢气,且越靠
(2)实验室制取二氧化碳:当其他因素都相同时,稀盐酸与粉末状石灰石反应速度大于与块状石灰石速率,由此可知化学反应速率快慢与
【设计实验】下表是他们分别用相同质量的Fe丝和足量稀硫酸反应的三组实验数据:
(3)实验②和③表明:该反应快慢与
(4)如果实验②反应的温度改为25℃,请推出Fe丝消失的时间(用t表示)的取值范围
【归纳总结】影响金属和稀硫酸反应快慢的因素主要有:反应物的种类,金属颗粒大小,反应温度以及
【拓展延伸】
(5)该实验除了用Fe丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量反应的快慢吗?方法:
(6)金属除了能和酸反应外还能和其他金属的盐溶液反应,已知下列各组物质间均能发生置换反应.
A.Fe和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式
②Mn、Fe、Mg、Cu四种金属的活动性由弱到强的顺序
查看习题详情和答案>>
【已有知识】
(1)根据金属的活动性顺序,只有排在氢(H)前面的金属才能与稀盐酸或稀硫酸反应制取氢气,且越靠
前
前
速率越快.(2)实验室制取二氧化碳:当其他因素都相同时,稀盐酸与粉末状石灰石反应速度大于与块状石灰石速率,由此可知化学反应速率快慢与
石灰石的颗粒大小
石灰石的颗粒大小
有关.【设计实验】下表是他们分别用相同质量的Fe丝和足量稀硫酸反应的三组实验数据:
| 实验编号 | 硫酸的质量分数/% | 反应的温度 | Fe丝消失的时间/S |
| ① | 3 | 20 | 500 |
| ② | 6 | 20 | 300 |
| ③ | 6 | 30 | 80 |
反应的温度
反应的温度
有关.(4)如果实验②反应的温度改为25℃,请推出Fe丝消失的时间(用t表示)的取值范围
80<t<300
80<t<300
.【归纳总结】影响金属和稀硫酸反应快慢的因素主要有:反应物的种类,金属颗粒大小,反应温度以及
稀硫酸的溶质质量分数
稀硫酸的溶质质量分数
等.【拓展延伸】
(5)该实验除了用Fe丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量反应的快慢吗?方法:
通过收集等量氢气所需时间来衡量反应的快慢
通过收集等量氢气所需时间来衡量反应的快慢
(6)金属除了能和酸反应外还能和其他金属的盐溶液反应,已知下列各组物质间均能发生置换反应.
A.Fe和CuSO4溶液 B.Mg和MnSO4溶液 C.Mn和FeSO4溶液
①写出Fe和CuSO4溶液反应的化学方程式
Fe+CuSO4═Cu+FeSO4
Fe+CuSO4═Cu+FeSO4
.②Mn、Fe、Mg、Cu四种金属的活动性由弱到强的顺序
Cu<Fe<Mn<Mg
Cu<Fe<Mn<Mg
.
实验探究是化学的灵魂,请你参与实验室制取氧气和二氧化碳的探究活动.
Ⅰ.制取氧气方法的分析
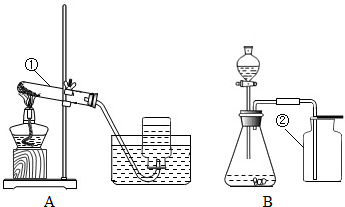
(1)写出A、B装置中标号仪器名称:① ;② .
(2)写出一个用A或B装置制取氧气的化学方程式 .
(3)若用B装置制取一瓶氧气,验满的方法是 .
(4)上述两种方法中,更符合“低碳”理念的是 (填“A”或“B”).
Ⅱ.制取二氧化碳原料的选择
(1)实验室常用大理石或石灰石(主要成分CaCO3)与稀盐酸反应制取二氧化碳,反应的化学方程式为 .
(2)实验过程中,同学们提出了下列问题并在老师指导下进行实验.
[问题一]能否用稀硫酸与块状石灰石反应制取二氧化碳?
[实验一]
[分析一]实验室 (填“能”或“不能”)用稀硫酸与块状石灰石反应制取二氧化碳.
[问题二]能否用粉末状的石灰石、碳酸钙粉末或碳酸钠粉末与稀盐酸反应制取二氧化碳?
[实验二]
[分析二]实验室不选用石灰石粉末、碳酸钙粉末或碳酸钠粉末制取二氧化碳的理由是 .
[结 论]实验室制取二氧化碳,原料通常用块状石灰石(或大理石)和稀盐酸.
[问题三]要得出该结论,上述两组对比实验中,[实验二]所取稀盐酸的体积是 mL、
溶质质量分数是 .
Ⅲ.拓展与反思
通过探究活动,你认为选择实验方法时应考虑的因素有 (写一种即可).
查看习题详情和答案>>
Ⅰ.制取氧气方法的分析

(1)写出A、B装置中标号仪器名称:①
(2)写出一个用A或B装置制取氧气的化学方程式
(3)若用B装置制取一瓶氧气,验满的方法是
(4)上述两种方法中,更符合“低碳”理念的是
Ⅱ.制取二氧化碳原料的选择
(1)实验室常用大理石或石灰石(主要成分CaCO3)与稀盐酸反应制取二氧化碳,反应的化学方程式为
(2)实验过程中,同学们提出了下列问题并在老师指导下进行实验.
[问题一]能否用稀硫酸与块状石灰石反应制取二氧化碳?
[实验一]
| 实验步骤 | 实验现象 |
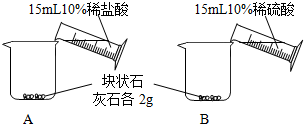 |
A中不断产生气泡,固体逐渐减少,有少量固体剩余. B中开始有少量气泡产生,反应很快停止. |
[问题二]能否用粉末状的石灰石、碳酸钙粉末或碳酸钠粉末与稀盐酸反应制取二氧化碳?
[实验二]
| 实验步骤 | 实验现象 |
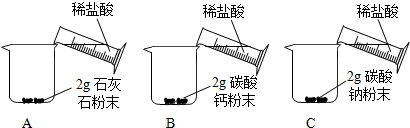 |
A中迅速产生大量气泡,固体很快减少,有少量固体剩余. B、C中都迅速产生大量气泡,固体很快消失. |
[结 论]实验室制取二氧化碳,原料通常用块状石灰石(或大理石)和稀盐酸.
[问题三]要得出该结论,上述两组对比实验中,[实验二]所取稀盐酸的体积是
溶质质量分数是
Ⅲ.拓展与反思
通过探究活动,你认为选择实验方法时应考虑的因素有