摘要:7.正常人的胃内的pH为1.2 - 3.0.当摄入过多的食物之后.将会引起胃酸的过多分泌.胃内的pH就会下降.使人有不适的感觉.胃药是为了减少胃内的盐酸的量.已知下列化合物都是无毒的.但是其中不能用作胃药的原料的是 A. AlCl3 B. Al(OH)3 C. NaHCO3 D. MgO
网址:http://m.1010jiajiao.com/timu3_id_281176[举报]
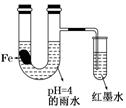
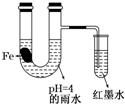 如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片.经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面.以下有关解释合理的是( )
如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片.经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面.以下有关解释合理的是( )
查看习题详情和答案>>
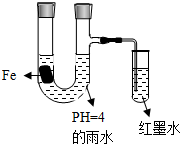 如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片.经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面.以下有关解释合理的是( )
如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片.经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面.以下有关解释合理的是( )| A、生铁片中的碳是原电池的负极,发生还原反应 | B、雨水酸性较强,生铁片始终发生析氢腐蚀 | C、墨水液面回升时,正极反应式为:O2+2H2O+4e-=4OH- | D、U型管中溶液pH逐渐减小 |
下图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是 ( )

A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水液面回升时,正极反应式为:O2 + 2H2O + 4e- = 4OH-
D.U型管中溶液pH逐渐减小
查看习题详情和答案>>
用氯气对饮用水消毒已有百年历史,但人们逐渐发现其副作用愈来愈明显:①pH的变化,对消毒能力影响大;②使饮用水中有机物发生氯代,生成上百种影响人体健康的有机氯衍生物,同时使人产生味觉、嗅觉不适感。世界环保联盟建议用另一种高效消毒剂二氧化氯(ClO2)代替氯气对饮用水消毒。ClO2具有很强的氧化性,通常状况下是黄绿色气体,水溶性是Cl2的5倍,溶于水成黄绿色的溶液,在pH为2~5范围内,在水中以分子形式存在,不水解,也不聚合。ClO2很不稳定,与空气混合后,当它的体积分数>10%时,受强光或强振动可能发生爆炸。
完成下列问题:?
(1)氯气对饮用水消毒的原理是________。氯气的消毒能力受水的pH影响,pH小时的消毒能力________pH大时的消毒能力(填“>”或“<”),其原因是________________________。?
(2)通常用氯酸钠(NaClO3)与浓盐酸反应来制取ClO2,同时生成Cl2,写出化学方程式:________________。市售的一种新型消毒剂含两种成分,分别是NaClO3和Na
某同学打算通过研究性学习,比较这两种制取ClO2的方法的利与弊。要拟定一个简略的研究方案,你认为应该从哪些方面进行研究?
__________________________________________
查看习题详情和答案>>