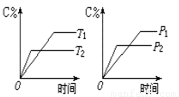
摘要:25.可逆反应mA pC.反应中.当其它条件不变时.C的质量分数与温度的关系如上图.根据图中曲线分析.判断下列叙述中正确的是 A.达到平衡后.若使用催化剂.C的质量分数增大 B.平衡后.若升高温度.则平衡向逆反应方向移动 C.平衡后.增大A的量.有利于平衡正向移动 D.化学方程式中一定有m+n<p+q
网址:http://m.1010jiajiao.com/timu3_id_280645[举报]
可逆反应mA(s)+nB(g)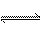 eC(g)+fD(g)反应过程中,当其他条件不变时,C的质量分数φ(C)的不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示。则下列叙述正确的是( )
eC(g)+fD(g)反应过程中,当其他条件不变时,C的质量分数φ(C)的不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示。则下列叙述正确的是( )
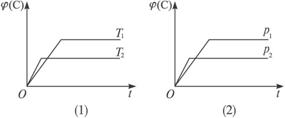
A.当平衡后,若温度升高化学平衡向逆反应方向移动
B.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
C.化学方程式中,m+n<e+f
D.达到平衡后,若使用催化剂C的质量分数将增大
查看习题详情和答案>>可逆反应mA(s)+nB(g) eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是(
)
eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是(
)
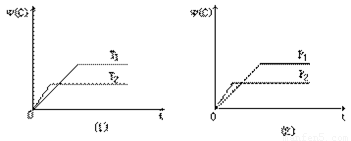
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.当平衡后,若温度升高,化学平衡向逆反应方向移动
C.化学方程式中,n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
查看习题详情和答案>>
可逆反应mA(s)+nB(g) pC(g);△H<0。在一定温度下,平衡时B的体积分数(B%)与压强的关系如图所示,下列叙述中一定正确的是:
pC(g);△H<0。在一定温度下,平衡时B的体积分数(B%)与压强的关系如图所示,下列叙述中一定正确的是: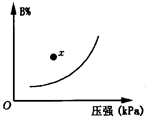
| A.m + n> p |
| B.升高温度平衡向正反应方向移动 |
| C.x点时正反应速率大于逆反应速率 |
| D.升高温度,逆反应速率增大,正反应速率减小 |
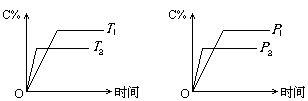
 pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是