网址:http://m.1010jiajiao.com/timu3_id_279596[举报]
汞(Hg)、铬(Cr)是影响环境污染、生物效应和人类健康的重金属元素。
I、铬广泛应用于钢铁工业、磁带和录像带等方面。
(1)工业常采用“铝在高温条件下还原铬绿(Cr2O3)”制备铬单质,该反应的化学方程式为 。
II、含铬的工业废水会导致慢性中毒。处理含+6价铬的废水时可得到铁氧体(其组成可写作[Fe2+Fe3+(2-x) Cr3+x]O4)。

(2)加过量FeSO4的目的是 。
(3)配平步骤①的反应的离子方程式 Fe2++ Cr2O72—+ _____== Fe3++ Cr3++ H2O
并计算铁氧体( [Fe2+Fe3+(2-x) Cr3+x]O4)中X= _________________。
(4)下表是实验检测中心对某地区二个点的土壤样品(每个点分三层取样,共6个样品)进行了有机质和铬总量的测定,结果见下表。
|
样品序号 |
取样深度(m) |
有机质(×10—2g) |
总铬(×10—6g) |
|
样品A-1 |
0.00 ~ 0.30 |
2.81 |
114 |
|
样品A-2 |
0.30 ~ 0.60 |
1.72 |
111 |
|
样品A-3 |
1.20 ~ 1.80 |
1.00 |
88 |
|
样品B-1 |
0.00 ~ 0.30 |
2.60 |
116 |
|
样品B-2 |
0.30 ~ 0.60 |
2.48 |
112 |
|
样品B-3 |
1.20 ~ 1.80 |
1.83 |
106 |
从表中你可以得出的结论有 (答一点即可)。
(5)工业上以铬酸钾(K2CrO4)为原料,电化学法制备重铬酸钾,装置如图。反应为:4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑已知K2CrO4铬酸钾溶液中存在平衡:2CrO42-(黄色)+2H+
2K2Cr2O7+4KOH+2H2↑+O2↑已知K2CrO4铬酸钾溶液中存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O通电后阳极区溶液由 变为
。原因是
。
Cr2O72-(橙色)+H2O通电后阳极区溶液由 变为
。原因是
。

查看习题详情和答案>>

(1)X的分子式为
(2)X分子中含有的官能团有
(3)X可能发生多种反应,下列有关X发生化学反应的叙述中正确的是
A.在氢氧化钠醇溶液中共热能发生消去反应
B.在铜作催化剂时加热,可被氧气氧化生成能发生银镜反应的物质
C.在浓硫酸存在时加热可发生消去反应
D.在铁作催化剂时,可跟液溴发生取代反应
(4)写出X跟氢氧化钠稀溶液共热时所发生反应的化学方程式
 +NaCl+H2O
+NaCl+H2O +NaCl+H2O
+NaCl+H2O(5)X可能有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式:


①苯环只有分子处在对位的两个取代基.
②遇氯化铁溶液不变色,但遇pH试纸显红色.
(12分)Ⅰ试写出中学阶段常见的两种制取氧气的化学方程式:
; 。
Ⅱ.实验室中通常用MnO2作催化剂分解过氧化氢,已知CuSO4溶液对过氧化氢的分解也具有催化作用,某实验兴趣小组同学猜想其他盐溶液也可能在这个反应中起同样的作用,于是他们做了以下探究。请你帮助他们完成实验报告:
(1)实验过程:在一支试管中加入5 mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。
实验现象: 。
实验结论:FeCl3溶液可以催化分解H2O2。
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-。
你认为最不可能的是 同学的猜想,理由是 。
(3)同学们对余下的两个猜想,用实验进行了探究,并记录如下,请你仔细分析后填表:
实验过程 实验现象 结论
| 实验过程 | 实验现象 | 结论 |
| 向盛有5 mL 5%的H2O2溶液的试管中滴入少量的 HCl,把带火星的木条伸入试管. | 无明显现象 | |
| 向盛有5 mL 5%的H2O2溶液的试管中滴入少量的Fe2(SO4)3,把带火星的木条伸入试管. | 试管中有大量气泡产生,带火星的木条复燃 | |
某有机物X是农药生产中的一种中间体,其结构简式为(如图)
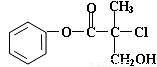
(1)X的分子式为____________
(2)X分子中含有的官能团有____________________(用结构简式表示)
(3)X可能发生多种反应,下列有关X发生化学反应的叙述中正确的是( )
A.在氢氧化钠醇溶液中共热能发生消去反应
B.在铜作催化剂时加热,可被氧气氧化生成能发生银镜反应的物质
C.在浓硫酸存在时加热可发生消去反应
D.在铁作催化剂时,可跟液溴发生取代反应
(4)写出X跟氢氧化钠稀溶液共热时所发生反应的化学方程式_________________________________。
(5)X可能有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式________ __。
①苯环只有分处在对位的两个取代基
②遇氯化铁溶液不变色,但遇pH试纸显红色
查看习题详情和答案>>
某有机物X是农药生产中的一种中间体,其结构简式为:
(1)X的分子式为_____________________________________。
(2)X分子中含有的官能团有________(用结构简式或名称表示均可)。

(3)X可能发生多种反应,下列有关X发生化学反应的叙述中正确的是________。
A.在氢氧化钠醇溶液中共热能发生消去反应;
B.在铜作催化剂时加热,可被氧气氧化生成能发生银镜反应的物质;
C.在浓硫酸存在时加热可发生消去反应;
D.在铁作催化剂时,可跟液溴发生取代反应;
(4)写出X跟氢氧化钠稀溶液共热时所发生反应的化学方程式________________。
(5)X可能有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式:
。
① 苯环只有分子处在对位的两个取代基。
查看习题详情和答案>>