摘要:13.某元素基态原子的电子排布式是[Ar]3d64s2.下列对该元素的说法中错误的是 A.该元素是过渡元素 B.该元素的化合价至少有+2.+3 C.该元素的单质不能与胆矾溶液反应 D.该元素的单质能与水蒸气反应
网址:http://m.1010jiajiao.com/timu3_id_279269[举报]
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,违反了泡利原理的是
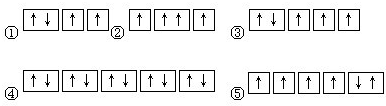
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
(3)用符号“>”、“<”或“=”表示下列各项关系.
①第一电离能:Na
②电负性:O
③能量高低:ns
④主族序数
查看习题详情和答案>>
②③
②③
,违反了洪特规则的是⑤
⑤
.
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
1s22s22p63s23p4
1s22s22p63s23p4
;其最高价氧化物对应水化物的化学式是H2SO4
H2SO4
.(3)用符号“>”、“<”或“=”表示下列各项关系.
①第一电离能:Na
<
<
Mg,Mg>
>
Ca.②电负性:O
<
<
F,F>
>
Cl.③能量高低:ns
<
<
(n+1)s,ns<
<
np.④主族序数
=
=
价电子数=
=
元素最高正化合价.下表为元素周期表的一部分,其中的编号代表对应的元素.

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)某元素原子的电子排布式为nsnnpn+1,该元素与元素①形成的分子遇到⑦与①形成的分子时的现象为
(4)元素⑨基态原子的电子排布式为
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
查看习题详情和答案>>

请回答下列问题:
(1)表中属于d区的元素是
⑨
⑨
(填编号).(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
苯
苯
.(3)某元素原子的电子排布式为nsnnpn+1,该元素与元素①形成的分子遇到⑦与①形成的分子时的现象为
产生白烟
产生白烟
;化学方程式为NH3+HCl=NH4Cl
NH3+HCl=NH4Cl
.(4)元素⑨基态原子的电子排布式为
1s22s22p63s23p63d64s2
1s22s22p63s23p63d64s2
,常见化合价是+2、+3
+2、+3
.(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
Be(OH)2+2NaOH=Na2BeO2+2H2O
Be(OH)2+2NaOH=Na2BeO2+2H2O
.下表列出了某短周期元素R的各级电离能数据(用I1、I2…表示,单位为kJ?mol-1).
|
查看习题详情和答案>>