摘要:15.① C<A<B,② B,增加溶质B使其达到饱和状态.蒸发溶剂水使其达到饱和状态. ③把混合物溶于水.升高溶液的温度.过滤.蒸发母液.
网址:http://m.1010jiajiao.com/timu3_id_2788[举报]
“冬天捞碱,夏天晒盐”.这里的“碱”是指Na2CO3,“盐”是指NaCl.
(一)Na2CO3和NaCl的溶解度曲线如图1所示,根据图回答:
①t1℃时Na2CO3的溶解度为 g;
t2℃时Na2CO3的溶解度 NaCl的溶解度.(填“<”、“>”或“=”)
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而 (填“增大”“减小”或“不变”).
③“夏天晒盐”是利用 (填序号)的方法,使NaCl晶体析出.
A.风吹日晒,使溶剂蒸发 B.升高温度,使NaCl溶解度增大
(二)我国青海湖地区得到的天然碱并不是碳酸钠的晶体,组成可表示为aNa2CO3?bNaHCO3?cH2O(a、b、c为最简整数比).某化学课外活动小组对天然碱的成分进行探究:
小红同学为测定其组成,称取该天然碱样品16.6g进行如图2实验: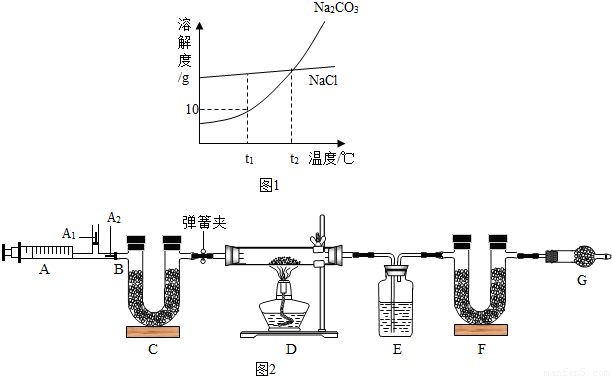
【查阅资料】
(1)碳酸钠比较稳定,加热时不分解;
(2)2NaHCO3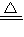 Na2CO3+CO2↑+H2O (3)图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
Na2CO3+CO2↑+H2O (3)图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
【实验步骤】
①组装好装置,检查气密性 ②反复推拉注射器 ③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行 ⑤打开弹簧夹,再次反复缓缓推拉注射器 ⑥再次称量E、F的质量.
【问题探究】
(1)E中的药品为 ,E的作用是 .
(2)C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是 ,F的作用是 ,G的作用是 .
(3)实验步骤②与③能否颠倒 (填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是
(4)据下表,16.6g天然碱中结晶水的质量为 g,Na2CO3的质量为 g,该天然碱的化学式中a:b:c= .
查看习题详情和答案>>
(一)Na2CO3和NaCl的溶解度曲线如图1所示,根据图回答:
①t1℃时Na2CO3的溶解度为 g;
t2℃时Na2CO3的溶解度 NaCl的溶解度.(填“<”、“>”或“=”)
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而 (填“增大”“减小”或“不变”).
③“夏天晒盐”是利用 (填序号)的方法,使NaCl晶体析出.
A.风吹日晒,使溶剂蒸发 B.升高温度,使NaCl溶解度增大
(二)我国青海湖地区得到的天然碱并不是碳酸钠的晶体,组成可表示为aNa2CO3?bNaHCO3?cH2O(a、b、c为最简整数比).某化学课外活动小组对天然碱的成分进行探究:
小红同学为测定其组成,称取该天然碱样品16.6g进行如图2实验:

【查阅资料】
(1)碳酸钠比较稳定,加热时不分解;
(2)2NaHCO3
 Na2CO3+CO2↑+H2O (3)图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
Na2CO3+CO2↑+H2O (3)图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.【实验步骤】
①组装好装置,检查气密性 ②反复推拉注射器 ③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行 ⑤打开弹簧夹,再次反复缓缓推拉注射器 ⑥再次称量E、F的质量.
【问题探究】
(1)E中的药品为 ,E的作用是 .
(2)C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是 ,F的作用是 ,G的作用是 .
(3)实验步骤②与③能否颠倒 (填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数 (填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是
(4)据下表,16.6g天然碱中结晶水的质量为 g,Na2CO3的质量为 g,该天然碱的化学式中a:b:c= .
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
下图是某研究性学习小组设计的几种装置,请分析并回答下列问题:

(1)用A装置可制取的气体是 ,化学反应方程式为 .
(2)B、C两装置都可用作实验室制取O2、H2或CO2的发生装置,写出用此两装置制取其中一种气体的化学方程式 .
(3)C装置是在B装置基础上增加隔离铜丝网改进而来的,它的优点是 .在实验室制取CO2时,若隔离网改用铝丝做成,那么产生的后果是 ,其原因是: ,说明金属活动性Cu Al(选填“>“、“<”或“=“)
(4)该研究性学习小组对用H2O2分解生成O2的实验条件进行探究,发现也可用Fe2O3代替MnO2,且用足量等体积H2O2溶液制取相同体积O2所需时间如下表:
MnO2、Fe2O3在上述反应中的作用是 .
从上表能得出的结论有① .
② .
(5)小童同学在使用“除垢净”去除热水瓶中的水垢时,发现有大量的气泡产生.联想水垢的主要成分是碳酸钙,小明猜想“除垢净”的成分中可能有酸.
①为证实自己的猜想,小童从家中又找来两类不同的物质进行实验:
实验一: ;
实验二: .
经实验,小童得出“除垢净”的有效成分中一定有酸的结论.
②小童想试制一瓶“除垢净”,你认为盐酸、硫酸这两种酸中的 更合适,理由是 .
③结合上面对“除垢净”的了解,在使用“除垢净”时应注意: .
查看习题详情和答案>>

(1)用A装置可制取的气体是
(2)B、C两装置都可用作实验室制取O2、H2或CO2的发生装置,写出用此两装置制取其中一种气体的化学方程式
(3)C装置是在B装置基础上增加隔离铜丝网改进而来的,它的优点是
(4)该研究性学习小组对用H2O2分解生成O2的实验条件进行探究,发现也可用Fe2O3代替MnO2,且用足量等体积H2O2溶液制取相同体积O2所需时间如下表:
| 浓度 时间 条件 |
30% H2O2溶液 | 15% H2O2溶液 | 5% H2O2溶液 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
从上表能得出的结论有①
②
(5)小童同学在使用“除垢净”去除热水瓶中的水垢时,发现有大量的气泡产生.联想水垢的主要成分是碳酸钙,小明猜想“除垢净”的成分中可能有酸.
①为证实自己的猜想,小童从家中又找来两类不同的物质进行实验:
实验一:
实验二:
经实验,小童得出“除垢净”的有效成分中一定有酸的结论.
②小童想试制一瓶“除垢净”,你认为盐酸、硫酸这两种酸中的
③结合上面对“除垢净”的了解,在使用“除垢净”时应注意:
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
查阅资料:
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵.
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示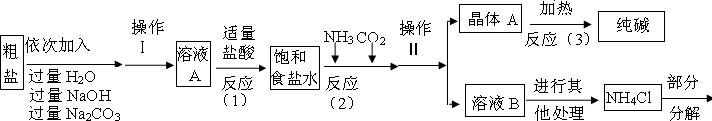
氯化铵分解的化学方程式是NH4Cl═NH3↑+HCl↑
<资料4>生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,分离的晶体A,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为 .
问题讨论:
(1)溶液A中的溶质为 ,操作Ⅱ的名称为 .
(2)上述流程中氢氧化钠溶液的作用是 ,碳酸钠溶液的作用是
(3)上述生产流程中可循环使用的是 (填序号).
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(4)上述反应(1)中发生了两个化学反应,写出反应的化学方程式: ,
组成确定:
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
由上述实验可确定纯碱样品含有杂质 (写化学式).
含量测定:
同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下实验.
甲组:取12,0g纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出.将反应后所得溶液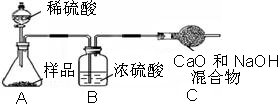 小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为 (必须要有写出计算过程,请在下方写出)
小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为 (必须要有写出计算过程,请在下方写出)
乙组:取12,0g纯碱样品,利用右图所示装置,测出反应后装置C增重了4.1g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是 .
丙组:取12.0克的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀后过滤、洗涤、烘干称量固体质量,从而计算碳酸钠的质量分数.组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是 .
查看习题详情和答案>>
查阅资料:
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵.
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示

氯化铵分解的化学方程式是NH4Cl═NH3↑+HCl↑
<资料4>生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,分离的晶体A,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为
问题讨论:
(1)溶液A中的溶质为
(2)上述流程中氢氧化钠溶液的作用是
(3)上述生产流程中可循环使用的是
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(4)上述反应(1)中发生了两个化学反应,写出反应的化学方程式:
组成确定:
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
由上述实验可确定纯碱样品含有杂质
含量测定:
同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下实验.
甲组:取12,0g纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出.将反应后所得溶液
 小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为
小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为乙组:取12,0g纯碱样品,利用右图所示装置,测出反应后装置C增重了4.1g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是
丙组:取12.0克的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀后过滤、洗涤、烘干称量固体质量,从而计算碳酸钠的质量分数.组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
查阅资料:
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱和氯化铵.
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示
氯化铵分解的化学方程式是NH4Cl═NH3↑+HCl↑
<资料4>生产原理:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,分离的晶体A,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为______.
问题讨论:
(1)溶液A中的溶质为______,操作Ⅱ的名称为______.
(2)上述流程中氢氧化钠溶液的作用是______,碳酸钠溶液的作用是______
(3)上述生产流程中可循环使用的是______(填序号).
A.CO2 B.NH3 C.HCl D.NaOH E.Na2CO3
(4)上述反应(1)中发生了两个化学反应,写出反应的化学方程式:______,______
组成确定:
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.
由上述实验可确定纯碱样品含有杂质______(写化学式).
含量测定:
同学们为了测定该纯碱样品的纯度(假定只含一种上述杂质),设计了如下实验.
甲组:取12,0g纯碱样品,向其中加入过量的盐酸,直至样品中无气泡冒出.将反应后所得溶液 小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为______(必须要有写出计算过程,请在下方写出)
小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为______(必须要有写出计算过程,请在下方写出)
乙组:取12,0g纯碱样品,利用右图所示装置,测出反应后装置C增重了4.1g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是______.
丙组:取12.0克的纯碱样品,完全溶于水,向其中加入过量的氯化钙溶液,待完全沉淀后过滤、洗涤、烘干称量固体质量,从而计算碳酸钠的质量分数.组内同学提出意见,认为如果将氯化钙溶液换成氯化钡溶液则更好,老师认为有道理,原因是______.
查看习题详情和答案>>
空气、水是人类赖以生存的自然资源.
(1)空气中主要含有氮气、氧气、稀有气体、二氧化碳等,按体积计算,其中含量最多的是______.人类时刻都离不开空气,是因为空气中的氧气能______.
(2)为了减慢大气中CO2含量的增加,以下建议可行的是(填序号)______.
①开发太阳能、水能、风能、地热等新能源;
②禁止使用煤、石油、天然气等矿物燃料;
③大量植树造林、禁止乱砍滥伐.
(3)下表为我国生活饮用水的标准:
| 感官指标 | 化学指标 | 细菌学指标 |
| 水质无色无味且澄清透明 | pH6.5~8.5; 总硬度<250mg/L(以碳酸钙计) 铜<1.0mg/L.…等 | 细菌总数<100个/mL等 |
②测定水样的酸碱度,可选用______(填序号);
A.酚酞溶液 B.pH试纸 C.石蕊溶液
③检验水样是硬水还是软水,可用的物质是______;
④漂白粉可用作水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2].次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O═CaCO3↓+2HClO,则X的化学式为______. 查看习题详情和答案>>