摘要:25.K2Cr2O7是橙红色晶体.K2CrO4是黄色晶体.若将K2Cr2O7配成一定浓度的溶液.可以发生的 离子反应方程式为:Cr2O2-7+H2O2CrO2-4+2H+.当达到平衡时.溶液的颜色在橙色和黄色之间.试回答: (1)向盛有2mL的上述K2Cr2O7溶液的试管中滴入10滴2mol·L-1的NaOH溶液.试管中溶呈 色.原因是 . 所得的溶液中滴入5滴2mol·L-1的硫酸.试管中溶液呈 色.理由是 .
网址:http://m.1010jiajiao.com/timu3_id_277771[举报]
化学平衡已知:重铬酸钾(K2Cr2O7)是橙红色晶体,铬酸钾(K2CrO4)是黄色晶体,重铬酸钾溶于水发生反应: Cr2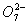 +H2O
+H2O 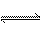 2Cr
2Cr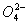 +2H+,溶液为橙黄色,向溶液中滴加少量稀硫酸,溶液呈_______色,向溶液中滴中少量KOH稀溶液,则溶液呈________色。
+2H+,溶液为橙黄色,向溶液中滴加少量稀硫酸,溶液呈_______色,向溶液中滴中少量KOH稀溶液,则溶液呈________色。
查看习题详情和答案>>
| |||||||||||||||||||||||