摘要:15.常温下.0.1mol·L-1的酸HA溶液的pH>1.0.1mol·L-1的碱BOH溶液中c(OH-):c(H+)=1012.将两溶液等体积混合.以下判断正确的是 A.HA是一种强酸 B.反应后BOH有剩余 C.反应后混合液呈中性 D.反应后混合液中还含有HA分子
网址:http://m.1010jiajiao.com/timu3_id_268870[举报]
常温下,0.1mol·L-1某一元酸HA溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是
- A.该溶液中由水电离出的c(H+)=1×10-11 mol·L-1
- B.由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中c(Na+)>c(A—)>c(OH―)>c(H+)
- C.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
- D.0.1mol·L-1HA溶液与0.05mol·L-1NaOH溶液等体积混合后所得溶液中2c(H+)+c(HA)=c(A-)+2c(OH-)
常温下,0.1mol·L—1某一元酸(HA)溶液中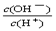 =1×10-8,下列叙述正确的是( )
=1×10-8,下列叙述正确的是( )
A.该一元酸溶液的pH=1 B.该溶液中HA的电离度为 1%
C.该溶液中水的离子积常数为1×10-14 D.若加水稀释,则c(OH-)/c(H+)将减小
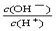 =1×10-8,下列叙述正确的是( )
=1×10-8,下列叙述正确的是( )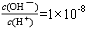 ,下列叙述正确是
,下列叙述正确是