摘要:2.了解:溶液的概念,溶质.溶剂的判断,饱和溶液与不饱和溶液的概念.判断.转换的方法,溶解度的概念,固体溶解度曲线的应用 ① 溶液的概念就是9个字:均一的.稳定的.混合物.溶液不一定是液体的.只要同时满足以上三个条件的物质.都可以认为是溶液. ② 一般简单的判断方法:当固体.气体溶于液体时.固体.气体是溶质.液体是溶剂.两种液体相互溶解时.通常把量多的一种叫做溶剂.量少的一种叫做溶质.当溶液中有水存在的时候.无论水的量有多少.习惯上把水看作溶剂.通常不指明溶剂的溶液.一般指的是水溶液. 在同一个溶液中.溶质可以有多种.特别容易判断错误的是.经过化学反应之后.溶液中溶质的判断. ③ 概念:饱和溶液是指在一定温度下.在一定量的溶剂里.不能再溶解某种物质的溶液.还能继续溶解某种溶质的溶液.叫做这种溶质的不饱和溶液. 在一定温度下.某溶质的饱和溶液只是说明在该温度下.不能够继续溶解该物质.但还可以溶解其他物质.比如说.在20℃的饱和氯化钠溶液中.不能再继续溶解氯化钠晶体.但还可以溶解硝酸钾固体. 判断:判断是否是饱和溶液的唯一方法:在一定温度下.继续投入该物质.如果不能继续溶解.则说明原溶液是饱和溶液.如果物质的质量减少.则说明原溶液是不饱和溶液. 当溶液中出现有固体时.则该溶液一定是该温度下.该固体的饱和溶液. 转换:饱和溶液与不饱和溶液的相互转换: 改变溶解度.实际一般就是指改变温度.但具体是升高温度还是降低温度.与具体物质溶解度曲线有 ④ 溶解度曲线的意义: (1)表示某物质在相应温度下的溶解度 (2)表示某物质在不同温度下的溶解度 (3)表示不同物质在同一温度下的溶解度 (4)表示某物质的溶解度随温度变化的趋势 ⑤ 溶解度曲线的应用: (1) 判断某一种物质在不同温度下的溶解度大小 (2) 比较同一温度下.不同物质溶解度的大小 (3) 判断不同物质溶解度受温度影响变化趋势 (4) 确定混合物的分离.提纯的方法 (5) 判断析出晶体量的多少 ⑥ 溶液中有关的计算公式: (1)溶解度的计算公式:溶解度= (2)溶液中溶质的质量分数= (3)饱和溶液的质量分数= 典型习题:
网址:http://m.1010jiajiao.com/timu3_id_26708[举报]
某化学小组为寻找分解过氧化氢溶液的新催化剂进行了如下探究活动.
[提出假设]:氧化铁可以做分解过氧化氢溶液的催化剂
[假设依据]:氧化铁和二氧化锰都属于金属氧化物,故性质相似.
[设计方案]:小组同学依据催化剂的概念设计实验方案.
实验一:探究氧化铁能否加快过氧化氢溶液分解的速率.
实验二:探究氧化铁的质量在反应前后是否变化.
实验三:探究氧化铁在反应前后化学性质是否改变.
[实验探究]:请你依据小组同学设计的实验方案,补充填写实验报告.
实验一:实验步骤如下图所示
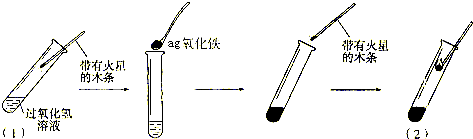
| 实验现象 | 结论 |
| (1) (2) |
| 实验步骤 | 实验现象 | 结论 |
| 待实验一完成后,将试管中的残余物小心过滤,并将全部滤渣洗涤、干燥、称量,观察是否仍为ag | 称重氧化铁的质量为ag |
| 实验步骤 | 实验现象 | 结论 |
| 将实验二的滤渣重新放入试管中,再加入少量过氧化氢溶液,并插入带火星木条,如此反复多次实验,观察现象 | 带火星木条复燃 |
[得出结论]______;
写出过氧化氢溶液在氧化铁作用下分解的化学方程式______. 查看习题详情和答案>>
(2006?宣武区二模)某化学小组为寻找分解过氧化氢溶液的新催化剂进行了如下探究活动.
[提出假设]:氧化铁可以做分解过氧化氢溶液的催化剂
[假设依据]:氧化铁和二氧化锰都属于金属氧化物,故性质相似.
[设计方案]:小组同学依据催化剂的概念设计实验方案.
实验一:探究氧化铁能否加快过氧化氢溶液分解的速率.
实验二:探究氧化铁的质量在反应前后是否变化.
实验三:探究氧化铁在反应前后化学性质是否改变.
[实验探究]:请你依据小组同学设计的实验方案,补充填写实验报告.
实验一:实验步骤如下图所示
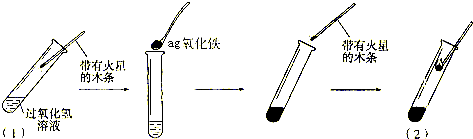
实验二:
实验三:
请你再设计一种实验方案,证明实验三的结论(若有反应发生,可用化学方程式表示)
[得出结论]
写出过氧化氢溶液在氧化铁作用下分解的化学方程式
查看习题详情和答案>>
[提出假设]:氧化铁可以做分解过氧化氢溶液的催化剂
[假设依据]:氧化铁和二氧化锰都属于金属氧化物,故性质相似.
[设计方案]:小组同学依据催化剂的概念设计实验方案.
实验一:探究氧化铁能否加快过氧化氢溶液分解的速率.
实验二:探究氧化铁的质量在反应前后是否变化.
实验三:探究氧化铁在反应前后化学性质是否改变.
[实验探究]:请你依据小组同学设计的实验方案,补充填写实验报告.
实验一:实验步骤如下图所示

| 实验现象 | 结论 |
| (1) (2) |
| 实验步骤 | 实验现象 | 结论 |
| 待实验一完成后,将试管中的残余物小心过滤,并将全部滤渣洗涤、干燥、称量,观察是否仍为ag | 称重氧化铁的质量为ag |
| 实验步骤 | 实验现象 | 结论 |
| 将实验二的滤渣重新放入试管中,再加入少量过氧化氢溶液,并插入带火星木条,如此反复多次实验,观察现象 | 带火星木条复燃 |
将滤渣放入盐酸中,观察实验现象.Fe2O3+6HCl=2FeCl3+3H2O
将滤渣放入盐酸中,观察实验现象.Fe2O3+6HCl=2FeCl3+3H2O
;[得出结论]
氧化铁可以做过氧化氢溶液分解的催化剂.
氧化铁可以做过氧化氢溶液分解的催化剂.
;写出过氧化氢溶液在氧化铁作用下分解的化学方程式
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
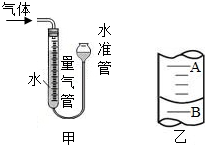
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)步骤①中的x应至少称取 g(结果保留1位小数),上述实验步骤中需要使用玻璃棒的是 (填序号).
(2)表格中的“待测数据”是指 .
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意 (填字母编号).
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为 .
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
查看习题详情和答案>>

①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | / | |
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
(1)步骤①中的x应至少称取
(2)表格中的“待测数据”是指
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:

①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)步骤①中的x应至少称取______g(结果保留1位小数),上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)表格中的“待测数据”是指______.
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意______(填字母编号).
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
查看习题详情和答案>>

①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | / | |
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
(1)步骤①中的x应至少称取______g(结果保留1位小数),上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)表格中的“待测数据”是指______.
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意______(填字母编号).
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
查看习题详情和答案>>
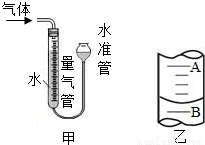
实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)步骤①中的x应至少称取______g(结果保留1位小数),上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)表格中的“待测数据”是指______.
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意______(填字母编号).
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
查看习题详情和答案>>

①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | / | |
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
(1)步骤①中的x应至少称取______g(结果保留1位小数),上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)表格中的“待测数据”是指______.
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意______(填字母编号).
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
查看习题详情和答案>>