摘要:27].将9.6g铜加入50 mL 12mol·L-1HNO3溶液中.待铜全部溶解后剩余溶液的pH=0.产生的气体(NO.NO2.N2O4中的一种或几种)折算成标准状况下的体积为4.48 L.请计算所得气体的成分及各成分的物质的量.
网址:http://m.1010jiajiao.com/timu3_id_263942[举报]
将9.6g铜加入50mL12mol?L-1的HNO3溶液中,待铜全部溶解后,剩余溶液中H+的浓度为1mol/L(忽略溶液体积的变化),产生的气体是NO、NO2、N2O4的混合气体,折算成标准状况下的体积为4.48L。请计算所得气体中各成分的物质的量。
查看习题详情和答案>>
金属铜能被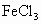 的浓溶液腐蚀.其化为反应是:
的浓溶液腐蚀.其化为反应是:
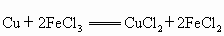 .
.
现将有铜的印刷线路板浸入120mL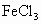 的溶液中,有9.6g铜被腐蚀掉,取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶物,则:①溶液中主要存在哪些离子?②离子的物质的量浓度各是多少(设溶液体积不变)?
的溶液中,有9.6g铜被腐蚀掉,取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶物,则:①溶液中主要存在哪些离子?②离子的物质的量浓度各是多少(设溶液体积不变)?
将6.4g 铜加入到50mL a mol/L的硝酸溶液中,铜全部溶解,得到NO2和NO的混合气体.将反应后溶液稀释至100mL,测得NO3-的浓度为3mol/L.
(1)混合气体中NO2和NO的总物质的量为
(2)稀释后的溶液中H+的物质的量浓度为
(3)若a=9,则混合气体中NO2的物质的量为
查看习题详情和答案>>
(1)混合气体中NO2和NO的总物质的量为
(0.05a-0.3)
(0.05a-0.3)
mol(用含a的式子表示).(2)稀释后的溶液中H+的物质的量浓度为
1
1
mol/L.(3)若a=9,则混合气体中NO2的物质的量为
0.125
0.125
mol.